Solubilisation par ultrasons de granulés de protéines
En protéomique, la préparation des échantillons n'est jamais un détail mineur. C'est la base sur laquelle reposent la précision de l'identification, la fiabilité de la quantification et la reproductibilité. L'un des défis les plus persistants dans la préparation des échantillons de protéines est la redissolution efficace des pastilles de protéines après les étapes de précipitation ou de concentration. C'est là que la solubilisation ultrasonique des culots de protéines est devenue de plus en plus importante. En appliquant une sonication contrôlée, les laboratoires peuvent améliorer la récupération des protéines, accélérer la dissolution des pastilles et préparer plus efficacement les échantillons pour la spectrométrie de masse et l'analyse biochimique en aval.
Solubilisation des protéines : L'importance de la sonication en protéomique moderne
Des culots de protéines se forment souvent lors de la précipitation à l'acétone, à l'éthanol, au méthanol-chloroforme, au sulfate d'ammonium ou au TCA. Ces flux de travail sont largement utilisés pour éliminer les contaminants, concentrer les protéines et purifier les extraits avant analyse. Cependant, une fois la précipitation terminée, le culot résultant peut être difficile à re-solubiliser. Les agrégats denses, les domaines hydrophobes, les protéines associées à la membrane et les complexes protéiques à forte interaction résistent souvent au mélange conventionnel ou au vortex. Une solubilisation incomplète peut alors entraîner une perte d'échantillon, une représentation biaisée des protéines et une mauvaise reproductibilité d'une expérience à l'autre.
La sonication s'attaque précisément à ce goulot d'étranglement. En générant de l'énergie mécanique dans un milieu liquide, la sonication perturbe les structures compactes des pastilles, favorise la pénétration des tampons et disperse les agrégats dans la solution. Il en résulte une reconstitution plus rapide et souvent plus complète des protéines, ce qui est particulièrement précieux lorsque l'on travaille avec des échantillons limités, des lysats complexes ou des cibles protéomiques difficiles.

Sonicateur pour microplaques UIP400MTP pour l'extraction des protéines et la solubilisation des granulés
Pourquoi les granulés de protéines sont-ils difficiles à solubiliser ?
 La précipitation des protéines est efficace car elle force les protéines à sortir de la solution. Cependant, le même processus qui rend la précipitation utile crée également le problème de la récupération des granulés. Une fois mises en boulettes, les protéines peuvent devenir très serrées et partiellement dénaturées. Les interactions hydrophobes peuvent s'intensifier, les liaisons intermoléculaires peuvent augmenter et certaines protéines peuvent piéger des sels, des lipides, des acides nucléiques ou d'autres composants de la matrice. Même lorsqu'un tampon de solubilisation puissant est utilisé, la remise en suspension passive est souvent lente et incomplète.
La précipitation des protéines est efficace car elle force les protéines à sortir de la solution. Cependant, le même processus qui rend la précipitation utile crée également le problème de la récupération des granulés. Une fois mises en boulettes, les protéines peuvent devenir très serrées et partiellement dénaturées. Les interactions hydrophobes peuvent s'intensifier, les liaisons intermoléculaires peuvent augmenter et certaines protéines peuvent piéger des sels, des lipides, des acides nucléiques ou d'autres composants de la matrice. Même lorsqu'un tampon de solubilisation puissant est utilisé, la remise en suspension passive est souvent lente et incomplète.
En protéomique, cela est important car une dissolution incomplète du culot ne réduit pas seulement le rendement total. Elle peut exclure sélectivement certaines classes de protéines, en particulier les protéines membranaires, les protéines structurelles ou les espèces sujettes à l'agrégation. Cela signifie que le résultat analytique final peut ne plus refléter la véritable composition de l'échantillon original. En protéomique à haute résolution, où de subtiles différences d'abondance ou de modification post-traductionnelle peuvent être biologiquement décisives, un tel biais de préparation constitue une sérieuse limitation.
Comment la sonication améliore la solubilisation des pastilles de protéines
Le traitement par ultrasons améliore la solubilisation en introduisant de l'énergie mécanique à haute fréquence dans l'échantillon. Cette énergie aide à briser le matériau compact du culot et augmente le contact entre le tampon de solubilisation et les protéines incorporées. Au lieu de s'appuyer uniquement sur la diffusion et le mélange manuel, le processus disperse activement le culot en fractions plus petites qui sont plus faciles à dissoudre.
L'effet pratique est important. La sonication peut :
- accélérer la dissolution des granulés de protéines denses ou récalcitrants
- améliorer la récupération des protéines peu solubles et agrégées
- réduire le temps de préparation dans les flux de travail de la protéomique
- favoriser des échantillons plus homogènes pour la digestion et l'analyse
Cette dispersion améliorée est particulièrement utile lorsque les pastilles sont remises en suspension dans des tampons contenant de l'urée, de la thiourée, des détergents, des chaotropes ou d'autres réactifs couramment utilisés en protéomique. La sonication permet à ces composants d'atteindre et de solubiliser le culot plus efficacement, ce qui permet d'obtenir une solution d'échantillon plus uniforme.
Avantages de la solubilisation ultrasonique en protéomique
Le principal avantage de la solubilisation par ultrasons est qu'elle transforme une étape de préparation souvent sous-estimée en un processus contrôlable et efficace. En protéomique, cela a des conséquences analytiques directes.
- Tout d'abord, une meilleure solubilisation augmente la probabilité que l'échantillon entrant dans la digestion enzymatique soit représentatif de l'ensemble des protéines. La digestion à la trypsine, par exemple, dépend des protéines qui sont correctement dépliées et accessibles en solution. Si des parties du culot restent non dissoutes, ces protéines sont effectivement exclues de la génération de peptides et donc de la détection.
- Deuxièmement, la sonication peut améliorer la reproductibilité. La remise en suspension manuelle des culots est intrinsèquement variable, en particulier lorsque différents opérateurs, tailles de culots ou matrices d'échantillons sont impliqués. Le traitement ultrasonique contrôlé normalise l'énergie physique appliquée à l'échantillon, ce qui peut réduire la variabilité entre les préparations et améliorer la cohérence des flux de travail LC-MS ou à base de gel en aval.
- Troisièmement, l'ultrasonication est très utile pour les échantillons précieux et à faible rendement. La protéomique clinique, la découverte de biomarqueurs, les expériences de culture cellulaire et les études de tissus reposent souvent sur un matériel limité. Toute perte de protéines au cours de la solubilisation réduit la valeur informative de l'échantillon. Une redissolution ultrasonique efficace permet de préserver autant d'analyte que possible.
- Enfin, la sonication accélère le flux de travail. Les laboratoires de protéomique qui traitent de nombreux échantillons ont besoin de méthodes de préparation robustes et rapides. Un culot qui se dissout rapidement et complètement n'est pas seulement pratique ; il réduit les délais, diminue le risque d'erreurs de manipulation et améliore le débit.
Sonication et méthodes conventionnelles de remise en suspension
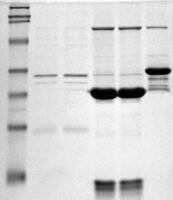 Les méthodes traditionnelles de remise en suspension des granulés impliquent généralement le pipetage, l'agitation, le vortex, une incubation prolongée ou des étapes de chauffage répétées. Si ces techniques peuvent fonctionner pour des granulés peu compacts, elles sont souvent difficiles à mettre en œuvre avec des protéines très compactes ou hydrophobes. Le mélange mécanique seul peut ne pas réussir à désintégrer complètement la structure du culot, laissant derrière lui des particules visibles ou des fractions insolubles invisibles.
Les méthodes traditionnelles de remise en suspension des granulés impliquent généralement le pipetage, l'agitation, le vortex, une incubation prolongée ou des étapes de chauffage répétées. Si ces techniques peuvent fonctionner pour des granulés peu compacts, elles sont souvent difficiles à mettre en œuvre avec des protéines très compactes ou hydrophobes. Le mélange mécanique seul peut ne pas réussir à désintégrer complètement la structure du culot, laissant derrière lui des particules visibles ou des fractions insolubles invisibles.
La sonication offre une approche plus active et plus ciblée. Plutôt que de dépendre de la diffusion lente du tampon, elle perturbe physiquement le culot et favorise une homogénéisation rapide. Cela n'élimine pas la nécessité d'un tampon de remise en suspension approprié, mais améliore considérablement les performances de ce tampon.
Par rapport aux méthodes purement manuelles, la solubilisation par ultrasons offre souvent un meilleur contrôle du processus, une plus grande efficacité et une meilleure adéquation aux applications protéomiques exigeantes. Pour les laboratoires qui recherchent à la fois la qualité analytique et la fiabilité opérationnelle, cela fait de la sonication un choix incontournable.
Les meilleurs cas d'utilisation pour la solubilisation ultrasonique des pastilles de protéines
La solubilisation par ultrasons est particulièrement bénéfique dans les flux de travail impliquant :
- précipitation des protéines avant la spectrométrie de masse,
- reconstitution de culots à partir de lysats cellulaires ou d'extraits de tissus,
- récupération des protéines riches en membrane ou sujettes à l'agrégation,
- et la préparation d'échantillons pour la protéomique quantitative où la reproductibilité est essentielle.
Elle est également très utile lorsque les pastilles ont été stockées, séchées trop fortement ou produites à partir de matrices biologiques complexes. Dans de tels cas, la remise en suspension passive peut devenir particulièrement inefficace, alors que la sonication permet de restaurer l'exploitabilité des échantillons avec moins d'intervention manuelle.

Sonicateur VialTweeter pour la sonication simultanée de 10 échantillons, par exemple pour l'extraction et la solubilisation de protéines
Trouvez le meilleur sonicateur pour votre flux de travail de solubilisation des protéines !
Pour les laboratoires travaillant avec des échantillons précieux, du matériel à faible débit ou de la protéomique à haut débit, le portefeuille de Hielscher offre plusieurs formats de sonication qui peuvent être adaptés précisément au flux de travail.
Que vous choisissiez un sonicateur à sonde Hielscher, le sonicateur multi-tubes VialTweeter ou le sonicateur pour microplaques UIP400MTP. – Chaque modèle d'ultrasoniseur répond à un scénario de préparation d'échantillons différent tout en partageant le même avantage principal : une énergie ultrasonique reproductible pour un traitement efficace et contrôlé des échantillons.
Sonicateurs à sonde
 Les sondes ultrasoniques telles que l'UP200Ht sont particulièrement bien adaptées à la sonication directe d'échantillons individuels. Pour les laboratoires de protéomique, l'UP200Ht est un choix judicieux lorsque des pastilles de protéines doivent être remises en suspension de manière intensive dans des volumes petits à moyens, en particulier lorsque le contrôle de la méthode et la répétabilité sont importants. La sonication directe de la sonde permet de désagréger rapidement les granulés compacts et d'aider les tampons de solubilisation à accéder aux protéines qui, autrement, resteraient partiellement non dissoutes.
Les sondes ultrasoniques telles que l'UP200Ht sont particulièrement bien adaptées à la sonication directe d'échantillons individuels. Pour les laboratoires de protéomique, l'UP200Ht est un choix judicieux lorsque des pastilles de protéines doivent être remises en suspension de manière intensive dans des volumes petits à moyens, en particulier lorsque le contrôle de la méthode et la répétabilité sont importants. La sonication directe de la sonde permet de désagréger rapidement les granulés compacts et d'aider les tampons de solubilisation à accéder aux protéines qui, autrement, resteraient partiellement non dissoutes.
Vue d'ensemble de tous les sonicateurs à sonde !
Sonicateur multi-tubes VialTweeter
 Lorsque plusieurs flacons fermés doivent être traités dans des conditions identiques, le Sonicateur Multi-Tube VialTweeter offre un avantage certain. Le VialTweeter permet une sonification intensive de petits volumes en sonifiant plusieurs flacons fermés dans des conditions stériles. La préparation simultanée d'échantillons dans plusieurs tubes à essai dans les mêmes conditions, ainsi que la réduction du risque de contamination croisée, de perte d'échantillons et de formation d'aérosols lors du traitement de flacons fermés font du VialTweeter un outil fiable pour la préparation d'échantillons. Pour la protéomique, cela est particulièrement important lors de la manipulation de culots précieux provenant de plusieurs réplicats ou d'échantillons cliniques, pour lesquels la cohérence entre les tubes est cruciale.
Lorsque plusieurs flacons fermés doivent être traités dans des conditions identiques, le Sonicateur Multi-Tube VialTweeter offre un avantage certain. Le VialTweeter permet une sonification intensive de petits volumes en sonifiant plusieurs flacons fermés dans des conditions stériles. La préparation simultanée d'échantillons dans plusieurs tubes à essai dans les mêmes conditions, ainsi que la réduction du risque de contamination croisée, de perte d'échantillons et de formation d'aérosols lors du traitement de flacons fermés font du VialTweeter un outil fiable pour la préparation d'échantillons. Pour la protéomique, cela est particulièrement important lors de la manipulation de culots précieux provenant de plusieurs réplicats ou d'échantillons cliniques, pour lesquels la cohérence entre les tubes est cruciale.
En savoir plus sur le VialTweeter !
Sonicateur pour microplaques UIP400MTP
 Pour les laboratoires à haut débit, le sonicateur de microplaques UIP400MTP étend les avantages de la sonication aux flux de travail basés sur les plaques. L'UIP400MTP est un sonicateur de microplaques et de plaques multi-puits permettant un traitement ultrasonique uniforme sur des plaques standard, y compris des formats à 96 puits, et souligne sa pertinence pour la préparation automatisée d'échantillons dans des domaines tels que la protéomique, le diagnostic et la découverte de médicaments. La plateforme est conçue pour le traitement simultané de nombreux échantillons, avec des avantages tels que la réduction du risque de contamination croisée, la diminution de l'intensité du travail, l'amélioration de la récupération des échantillons et l'intégration dans des flux de travail automatisés.
Pour les laboratoires à haut débit, le sonicateur de microplaques UIP400MTP étend les avantages de la sonication aux flux de travail basés sur les plaques. L'UIP400MTP est un sonicateur de microplaques et de plaques multi-puits permettant un traitement ultrasonique uniforme sur des plaques standard, y compris des formats à 96 puits, et souligne sa pertinence pour la préparation automatisée d'échantillons dans des domaines tels que la protéomique, le diagnostic et la découverte de médicaments. La plateforme est conçue pour le traitement simultané de nombreux échantillons, avec des avantages tels que la réduction du risque de contamination croisée, la diminution de l'intensité du travail, l'amélioration de la récupération des échantillons et l'intégration dans des flux de travail automatisés.
Dans la pratique de la protéomique, cela signifie que la solubilisation du culot, la lyse cellulaire, l'extraction et les étapes de préparation connexes peuvent être mises à l'échelle de manière beaucoup plus efficace. Plutôt que de traiter les échantillons un par un, les laboratoires peuvent soniquer des plaques entières avec un apport d'énergie constant. Cet avantage est précieux lorsque les flux de travail doivent combiner débit et rigueur analytique, par exemple dans le cadre d'études de criblage, de protéomique quantitative ou de pipelines de préparation d'échantillons standardisés. L'UIP400MTP n'est donc pas seulement un outil pratique ; c'est une plate-forme qui soutient la tendance générale vers l'automatisation, la reproductibilité et la protéomique robuste à haut débit.
En savoir plus sur le sonificateur de microplaques UIP400MTP !

VialTweeter dans la chambre de réfrigération – les paramètres contrôlés du processus pendant la sonication.

Extraction et solubilisation de protéines à haut débit avec le sonicateur de microplaques UIP400MTP
Conception, fabrication et conseil – Qualité Made in Germany
Les ultrasons Hielscher sont réputés pour leur qualité et leurs normes de conception les plus élevées. La robustesse et la facilité d'utilisation permettent une intégration aisée de nos ultrasons dans les installations industrielles. Les conditions difficiles et les environnements exigeants sont facilement gérés par les ultrasons Hielscher.
Hielscher Ultrasonics est une entreprise certifiée ISO et met l'accent sur les ultrasons de haute performance, dotés d'une technologie de pointe et d'une grande facilité d'utilisation. Bien entendu, les ultrasons Hielscher sont conformes à la norme CE et répondent aux exigences des normes UL, CSA et RoHs.
Littérature / Références
- FactSheet UIP400MTP Plate-Sonicator for High-Throughput Sample Preparation – English version – Hielscher Ultrasonics
- FactSheet VialTweeter – Sonicator for Simultaneous Sample Preparation
- Susana Jorge, Kevin Pereira, Hugo López-Fernández, William LaFramboise, Rajiv Dhir, Javier Fernández-Lodeiro, Carlos Lodeiro, Hugo M. Santos, Jose L. Capelo-Martínez (2020): Ultrasonic-assisted extraction and digestion of proteins from solid biopsies followed by peptide sequential extraction hyphenated to MALDI-based profiling holds the promise of distinguishing renal oncocytoma from chromophobe renal cell carcinoma. Talanta, Volume 206, 2020.
- Lindemann C, Lupilova N, Müller A, Warscheid B, Meyer HE, Kuhlmann K, Eisenacher M, Leichert LI. (2013): Redox proteomics uncovers peroxynitrite-sensitive proteins that help Escherichia coli to overcome nitrosative stress. Journal of Biological Chemistry 288(27); 2013. 19698-714.
- Gonçalo Martins, Javier Fernández-Lodeiro, Jamila Djafari, Carlos Lodeiro, J.L. Capelo, Hugo M. Santos (2019): Label-free protein quantification after ultrafast digestion of complex proteomes using ultrasonic energy and immobilized-trypsin magnetic nanoparticles. Talanta, Volume 196, 2019. 262-270.
Questions fréquemment posées
Pourquoi les bains à ultrasons ne conviennent-ils pas à la solubilisation des protéines ?
Dans les bains à ultrasons, la cavitation, principe de fonctionnement de la sonication, se produit de manière très irrégulière, soumettant les échantillons à des traitements de sonication variables. Selon la position des tubes à échantillons dans le bain à ultrasons, chaque échantillon est soumis à des intensités différentes. La protéomique dépend de la comparabilité. Si un culot est incomplètement dissous alors qu'un autre est entièrement remis en suspension, les données qui en résultent peuvent refléter un biais de préparation plutôt qu'une véritable biologie. Contrairement aux bains ultrasoniques, les sonicateurs sans contact tels que le VialTweeter ou le Microplate Sonicator UIP400MTP permettent une manipulation plus standardisée en permettant à plusieurs échantillons d'être traités en parallèle dans les mêmes conditions ultrasoniques, ce qui peut contribuer à améliorer la reproductibilité entre les expériences. Ceci est particulièrement utile dans les études de biomarqueurs, la protéomique comparative et les flux de travail avec de multiples réplicats biologiques ou techniques.
Quels sont les essais les plus courants en protéomique ?
Les essais les plus courants en protéomique sont les essais de quantification des protéines et les méthodes de caractérisation des protéines utilisées lors de la préparation et de l'analyse des échantillons. Les tests les plus fréquemment utilisés sont le test de Bradford, le test BCA, le test de Lowry et l'absorbance UV à 280 nm pour la mesure de la concentration en protéines. Dans les flux de travail plus larges de la protéomique, les analyses SDS-PAGE, Western blotting, ELISA, la digestion dans le gel et les analyses basées sur la spectrométrie de masse sont également largement utilisées pour évaluer l'abondance, la pureté, le poids moléculaire et l'identité des protéines.
Qu'est-ce que le bleu brillant de Coomassie ?
Le bleu brillant de Coomassie est un colorant à base de triphénylméthane largement utilisé dans la science des protéines pour la coloration des protéines dans les gels et pour la quantification colorimétrique des protéines. Il se lie principalement aux résidus d'acides aminés basiques et aromatiques, en particulier l'arginine, et subit un déplacement spectral lorsqu'il se lie aux protéines. Cette propriété le rend utile à la fois pour la visualisation des protéines après électrophorèse et pour le test protéique de Bradford.
Comment fonctionne le test de Bradford ?
Le test de Bradford consiste à mélanger un échantillon de protéines avec du colorant bleu brillant de Coomassie dans des conditions acides. Lorsque le colorant se lie aux protéines, son maximum d'absorbance passe d'environ 465 nm à 595 nm, ce qui provoque un changement de couleur mesurable du brun rougeâtre au bleu. L'augmentation de l'absorbance à 595 nm est proportionnelle à la concentration en protéines dans une plage définie, ce qui permet de la quantifier par comparaison avec une courbe standard, généralement préparée avec de l'albumine sérique bovine.

Hielscher Ultrasonics fabrique des homogénéisateurs à ultrasons très performants à partir de laboratoires à taille industrielle.


