Ultraschall-Liposomen-Verkapselung von GLP-1-Peptiden: Skalierbare Technologie für die orale Peptidverabreichung
Semaglutid und andere GLP-1-Peptide verändern die Diabetes- und Adipositasbehandlung, aber die meisten Peptidmedikamente müssen immer noch gespritzt werden, da die orale Verabreichung eine große Herausforderung darstellt. Selbst das zugelassene orale Semaglutid weist eine Bioverfügbarkeit von weniger als 1 % auf, was den Dosisbedarf und die Kosten erhöht. Die Verkapselung von GLP-1-Peptiden in Liposomen kann diese Einschränkungen überwinden. Erfahren Sie, wie die Ultraschall-Liposomenzubereitung GLP-1-Peptid-haltige Liposomen in Compounding-Apotheken und in der pharmazeutischen Produktion erleichtert.
Liposomale GLP-1-Peptide
GLP-1-Rezeptor-Agonisten wie Semaglutid und Inkretin-Peptide der nächsten Generation wie Tirzepatid haben die Behandlung von Typ-2-Diabetes und Adipositas verändert. Aus Sicht der Formulierung und Herstellung weisen diese Wirkstoffe jedoch immer noch die klassischen Einschränkungen von Peptidmedikamenten auf: Sie sind empfindlich, werden leicht abgebaut und lassen sich nur schwer durch den Magen-Darm-Trakt verabreichen.
Aus diesem Grund werden die meisten GLP-1-Peptide nach wie vor injiziert, obwohl die orale Verabreichung die Hürden für die Patienten drastisch senken würde. Die orale Verabreichung verbessert im Allgemeinen die Bequemlichkeit, die Therapietreue und die Bereitschaft, die Therapie früher zu beginnen – insbesondere bei chronischen Krankheiten.
Die orale Verabreichung von Peptiden bleibt jedoch eine der schwierigsten Herausforderungen in der pharmazeutischen Wissenschaft. Selbst zugelassene orale Semaglutid-Produkte weisen eine sehr geringe Bioverfügbarkeit auf und erfordern hohe Dosierungen und sorgfältige Formulierungsstrategien.
Einer der vielversprechendsten technischen Ansätze zur Überwindung dieser Beschränkungen ist die liposomale Verkapselung in Kombination mit hochintensiver Ultraschallverarbeitung. Liposomen schützen peptidische Wirkstoffe, verbessern die Dispersionsstabilität und können in Größenordnungen im Nanobereich hergestellt werden, die für die Schleimdurchdringung und die Interaktion mit dem Darm relevant sind. Die Sonikation bietet eine skalierbare und reproduzierbare Methode zur Herstellung dieser Liposomen in industriell relevanten Mengen.
Warum Liposomen eine starke Plattform für GLP-1-Peptide sind
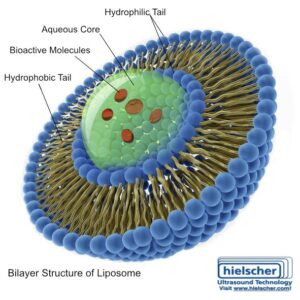 Liposomen sind Vesikel, die aus Phospholipid-Doppelschichten bestehen und in ihrer Zusammensetzung biologischen Membranen ähneln. Dadurch sind sie von Natur aus biokompatibel und eignen sich gut für die pharmazeutische Entwicklung. Für Peptidarzneimittel sind Liposomen attraktiv, weil sie den Wirkstoff physisch schützen können und eine Formulierungsarchitektur bieten, die auf die Abgabeleistung abgestimmt werden kann.
Liposomen sind Vesikel, die aus Phospholipid-Doppelschichten bestehen und in ihrer Zusammensetzung biologischen Membranen ähneln. Dadurch sind sie von Natur aus biokompatibel und eignen sich gut für die pharmazeutische Entwicklung. Für Peptidarzneimittel sind Liposomen attraktiv, weil sie den Wirkstoff physisch schützen können und eine Formulierungsarchitektur bieten, die auf die Abgabeleistung abgestimmt werden kann.
Im Zusammenhang mit GLP-1-Peptiden besteht die zentrale Herausforderung nicht nur darin, das Peptid vor Säure und Enzymen zu schützen, sondern auch eine sinnvolle Aufnahme durch die Darmbarriere zu ermöglichen. Dies ist ein vielschichtiges Problem, das den pH-Wert, den enzymatischen Abbau, den Schleimtransport, die epitheliale Permeabilität und die Transportmechanismen einbezieht.
In der wissenschaftlichen Literatur wird zunehmend der Gedanke unterstützt, dass Träger auf Vesikelbasis die Stabilität von Peptiden und ihre Interaktion mit dem Darmsystem verbessern können.
Warum Semaglutid für die liposomale Verkapselung besonders interessant ist
Semaglutid ist nicht nur ein Peptid – es ist ein Peptid mit einer eingebauten Lipidschwanzmodifikation. Dies ist ein wesentlicher Grund dafür, dass es sich in Lipidsystemen anders verhält als viele andere Peptidwirkstoffe.
GLP-1-Peptide wie Semaglutid und Tirzepatid werden über eine Lipidschwanz-Insertion in die Vesikelmembran geladen.
Aus technischer Sicht ist dies wichtig, weil es darauf hindeutet, dass Semaglutid strukturell mit Lipiddoppelschichten kompatibel ist, was bedeutet, dass es möglich sein könnte, eine stabile Assoziation und eine sinnvolle Beladung ohne übermäßige chemische Veränderungen zu erreichen.
Diese Logik gilt auch für andere lipidierte Peptidwirkstoffe und Peptid-Wirkstoff-Konjugate.
Die Herstellungsrealität: Liposomen müssen reproduzierbar und skalierbar sein
Die Verkapselung von Liposomen ist in einem Labor nicht schwierig. Die eigentliche Schwierigkeit beginnt, wenn eine Formulierung in reproduzierbarem Umfang hergestellt werden muss.
Die industrielle Liposomenproduktion muss kontrolliert werden:
- Liposomengrößenverteilung
- Polydispersität
- Verkapselungseffizienz
- Dispersionsstabilität
- Reproduzierbarkeit von Charge zu Charge
- Kompatibilität mit Sterilgutaufbereitung
- Prozessvalidierung und -dokumentation
Viele gängige Liposomen-Methoden (Vortexen, einfache Hydratisierung, Handextrusion) können im Labor gute Ergebnisse liefern, versagen aber, wenn sie in Pilot- oder Produktionsmengen eingesetzt werden.
Hier wird die Ultraschallbearbeitung zu einer Schlüsseltechnologie.
Liposomenverkapselung mit Ultraschall: Das Grundprinzip
Mit hochintensivem Ultraschall wird über akustische Kavitation mechanische Energie in eine Flüssigkeit eingebracht. Kavitation ist die Bildung und das Kollabieren von mikroskopisch kleinen Blasen, die lokale Scherkräfte und Mikrovermischungseffekte erzeugen.
In Lipiddispersionen sind diese Kräfte:
- Herstellung von Mikroemulsionen zur Einleitung der Liposomenbildung
- große Lipidaggregate abbauen
- multilamellare Strukturen reduzieren
- kleinere, einheitlichere Bläschen erzeugen
- Homogenisierung verbessern
- die Reproduzierbarkeit der fertigen Dispersion zu erhöhen
Ultraschallverfahren werden daher häufig bei der Herstellung, Emulgierung und Dispersion von Nanomaterialien eingesetzt und eignen sich hervorragend für die Nanogröße von Liposomen.
Bei GLP-1-Peptid-Liposomen kann Ultraschall entweder direkt während der Hydratation und Dispersion zur Herstellung von Liposomen oder als Nachbearbeitungsschritt zur Verfeinerung der Vesikelgröße und Verbesserung der Einheitlichkeit eingesetzt werden.
Warum Ultraschall für die Herstellung pharmazeutischer Liposomen besonders wertvoll ist
Der wichtigste Grund für den industriellen Einsatz von Ultraschall ist, dass er durch die Kontrolle eines messbaren Prozessparameters skaliert werden kann: Energie pro Volumen.
Anstatt einer Skalierung um „Mehr Mischen“ oder „längere Bearbeitung,“ Ultraschallsysteme ermöglichen die Skalierung des Prozesses um:
- Erhöhung der Ultraschallleistung
- Erhöhung der Durchflussmenge
- Beibehaltung des gleichen Energieinputs pro mL
- Verwendung von Durchflussreaktoren
- Parallelnummerierung
Dies macht das Verfahren in hohem Maße übertragbar von R&D zur Produktion.
In der Praxis bedeutet dies, dass ein Liposomenprozess, der auf einem kleinen System entwickelt wurde, auf größere Systeme übertragen werden kann, wobei gleichwertige Prozessbedingungen beibehalten werden, was genau den Anforderungen der pharmazeutischen Produktion entspricht.
Die Auswirkungen auf GLP-1-Peptide: Auf dem Weg zu einer besseren oralen Bioverfügbarkeit
Die orale Verabreichung ist das langfristige Ziel für viele GLP-1-Peptidformulierungen. Der Grund ist einfach: Wenn sich die orale Bioverfügbarkeit verbessert, wird die gesamte Therapie für die Patienten einfacher.
Das von Ihnen hochgeladene Material verdeutlicht die derzeitige Einschränkung: Semaglutid kann zwar oral eingenommen werden, aber die Bioverfügbarkeit bleibt gering (unter 1 %).
Die Liposomenverkapselung ist keine Garantie für eine hohe orale Bioverfügbarkeit, aber sie behebt mehrere kritische Engpässe gleichzeitig:
- Es kann das Peptid physisch vor dem Abbau schützen.
- Sie kann nanoskalige Träger mit auf die Schleimdurchdringung abgestimmten Eigenschaften erzeugen.
- Es kann mit Oberflächenliganden für aktive Transportmechanismen funktionalisiert werden.
- Sie kann die Konsistenz und Reproduzierbarkeit der gelieferten Wirkstoffform verbessern.
Insbesondere für Semaglutid bietet die Membranassoziation über den Lipidschwanz einen zusätzlichen Mechanismus, der das Peptid in Lipidsystemen stabilisieren kann.
Ultraschallverfahren ermöglicht kontinuierliche, industrielle Liposomenproduktion
In der industriellen Fertigung wird die kontinuierliche Verarbeitung häufig bevorzugt, weil sie die Qualität verbessert:
- Durchsatz
- Reproduzierbarkeit
- Präzise Prozesssteuerung
- Integration in sterile Produktionsabläufe
Ultraschall-Durchflusssysteme sind hierfür ideal. Die Liposomendispersion wird durch eine druckbeaufschlagte Durchflusszelle gepumpt, in der unter kontrollierten Bedingungen Ultraschall angewendet wird. Temperatur, Druck und Verweilzeit können gesteuert werden, was für Peptidformulierungen von entscheidender Bedeutung ist.
Dies ermöglicht skalierbare Arbeitsabläufe für die Nanogröße und Verkapselung, die den GMP-Anforderungen weitaus näher kommen als viele reine Laborverfahren.
Hielscher-Ultraschall: Lab-to-Industrial-Systeme für die Liposomenverkapselung

Hielscher Ultrasonics bietet Ultraschallsysteme an, die dem realen Entwicklungspfad von liposomalen Peptidformulierungen entsprechen.
Im Labormaßstab wird das UP400St häufig für das Formulierungsscreening, die Prozessentwicklung und die Herstellung von Liposomen im Compounding-Maßstab verwendet.
Im Produktionsmaßstab sind UIP2000hdT und UIP4000hdT für industrielle Arbeitszyklen ausgelegt und können mit Durchflussbeschallungszellen für die kontinuierliche Verarbeitung integriert werden.
Diese Kombination ist für die Herstellung pharmazeutischer Liposomen besonders wichtig, da sie die Produktion unterstützt:
- Reproduzierbarkeit der Prozesse
- lineare Skalierbarkeit
- Fließfertigung
- Hochleistungs-Ultraschallbearbeitung unter kontrollierten Bedingungen

Sonicator UIP1000hdT mit Glasdurchflusszelle für die Herstellung von Liposomen.
Auf einen Blick – Warum die Ultraschall-Liposomen-Formulierung von GLP-1-Peptiden
Die Ultraschall-Liposomenverkapselung ist einer der technisch ausgereiftesten und industriell skalierbaren Ansätze für die Herstellung peptidbeladener Liposomen. Für GLP-1-Peptide wie Semaglutid und Tirzepatid ist dieser Ansatz besonders relevant, da diese Wirkstoffe strukturell mit Lipidmembranen kompatibel sind und von vesikelbasierten Schutz- und Lieferstrategien profitieren können.
Am wichtigsten ist, dass Ultraschall nicht nur eine Labormethode ist. – es ist eine skalierbare Prozesstechnologie. Durch die Steuerung des Energieeintrags pro Volumen und die Verwendung von Durchflussbeschallungszellen kann die Ultraschallverarbeitung von der Entwicklung im Labormaßstab auf die Pilot- und vollständige industrielle Produktion übertragen werden.
Die pharmazeutische Industrie entwickelt sich weiter in Richtung Peptidtherapeutika – und da die Nachfrage nach patientenfreundlichen Lieferwegen wächst – Die Herstellung von Liposomen im Ultraschallverfahren wird eine immer wichtigere Rolle bei der nächsten Generation von GLP-1-Formulierungen spielen.
In der folgenden Tabelle finden Sie die ungefähre Verarbeitungskapazität unserer Ultraschallhomogenisatoren:
| Batch-Volumen | Durchfluss | Empfohlenes Ultraschallgerät |
|---|---|---|
| 0,5 bis 1,5 ml | n.a. | VialTweeter |
| 1 bis 500ml | 10 bis 200ml/min | UP100H |
| 10 bis 2000ml | 20 bis 400ml/min | UP200Ht, UP400St |
| 0.1 bis 20l | 0,2 bis 4l/min | UIP2000hdT |
| 10 bis 100l | 2 bis 10l/min | UIP4000hdT |
| 15 bis 150 Liter | 3 bis 15 l/min | UIP6000hdT |
| n.a. | 10 bis 100l/min | UIP16000hdT |
| n.a. | größere | Cluster aus UIP16000hdT |
Design, Herstellung und Beratung – Qualität Made in Germany
Hielscher Ultraschallgeräte sind bekannt für höchste Qualität und Designstandards. Robustheit und einfache Bedienung ermöglichen die problemlose Integration unserer Ultraschallgeräte in industrielle Anlagen. Raue Bedingungen und anspruchsvolle Umgebungen sind für Hielscher Ultraschallgeräte kein Problem.
Hielscher Ultrasonics ist ein ISO-zertifiziertes Unternehmen und legt großen Wert darauf, Hochleistungs-Ultraschallgeräte zu entwickeln und zu produzieren, die sich durch modernste Technik und Benutzerfreundlichkeit auszeichnen. Selbstverständlich sind Hielscher Sonicators CE-konform und erfüllen die Anforderungen von UL, CSA und RoHs.
Literatur / Literaturhinweise
- Martyna Truszkowska; Ahmad Saleh; Melanie Lena Eber; Gergely Kali; Andreas Bernkop-Schnürch (2025): Addressing the polycation dilemma in drug delivery: charge-converting liposomes. Journal of Materials Chemistry B 2025, 13, 9100-9111.
- Pop, R.; Nistor, M.; Socaciu, C.; Cenariu, M.; Tăbăran, F.; Rugină, D.; Pintea, A.; Socaciu, M.A. (2025): Distinct In Vitro Effects of Liposomal and Nanostructured Lipid Nanoformulations with Entrapped Acidic and Neutral Doxorubicin on B16-F10 Melanoma and Walker 256 Carcinoma Cells. Pharmaceutics 2025, 17, 904.
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
Häufig gestellte Fragen
Welche Rolle spielt die Ultraschallemulgierung bei der Bildung von Liposomen?
Die Emulgierung der wässrigen Phase und der Lipide mit Ultraschall liefert die mechanische Energie, die erforderlich ist, um die Lipide fein in Wasser zu dispergieren und ihre Selbstorganisation zu geschlossenen Doppelschichtstrukturen zu fördern. Die durch Ultraschall erzeugte akustische Kavitation erzeugt intensive Mikrovermischungs- und Scherkräfte, die Lipidphasen fragmentieren, Lipidmoleküle gleichmäßig hydratisieren und dispergierte Lipidfragmente in liposomale Vesikel umwandeln. Dies fördert die schnelle Vesikelbildung, reduziert multilamellare Strukturen und führt zu kleineren, einheitlicheren Liposomen mit besserer Reproduzierbarkeit und Stabilität.
Was sollte ich über die GLP-1-Formulierung wissen?
GLP-1-Peptide sind hochwirksame Medikamente, doch die meisten von ihnen können aufgrund des Abbaus im Magen-Darm-Trakt und der Absorptionsbarrieren nur injiziert werden.
Semaglutid zum Einnehmen gibt es bereits, aber die gemeldete Bioverfügbarkeit liegt unter 1 %.
Semaglutid und Tirzepatid können in Vesikelsysteme geladen werden, wobei die Ladeeffizienz stark von der Verarbeitungsmethode abhängt.
Semaglutid kann über seinen Lipidschwanz mit Lipidmembranen assoziieren, was die Kompatibilität von Vesikeln und Liposomen unterstützt.
Die Ultraschallkavitation ermöglicht eine reproduzierbare Nanogröße der Liposomen und eine Homogenisierung der Dispersion.
Ultraschall skaliert linear durch Energie-pro-Volumen-Steuerung und kontinuierliche Flussverarbeitung.
Hielscher-Systeme unterstützen den gesamten Workflow:
- UP400St (Labor- und Mischungswaage)
- UIP2000hdT / UIP4000hdT + Durchflusszellen (industrielle pharmazeutische Herstellung)
Was sind GLP-1-Peptide?
GLP-1-Peptide sind Inkretinrezeptor-Agonisten auf Peptidbasis, die die biologische Aktivität von Glucagon-like Peptide-1 (GLP-1), einem Darmhormon, das an der glukoseabhängigen Insulinsekretion, der Unterdrückung der Glucagonausschüttung und der Regulierung der Magenentleerung und des Appetits beteiligt ist, nachahmen oder verstärken. Klinisch verwendete GLP-1-Medikamente (z. B. Semaglutid) sind chemisch modifiziert, um dem enzymatischen Abbau zu widerstehen und eine lange systemische Halbwertszeit zu erreichen.
Wie werden GLP-1-Peptide üblicherweise verabreicht?
Die meisten GLP-1-Peptide werden durch subkutane Injektion verabreicht, da die Peptide im Magen-Darm-Trakt instabil sind und eine extrem geringe intestinale Permeabilität aufweisen. Semaglutid kann mithilfe spezieller Formulierungsstrategien oral verabreicht werden, doch die orale Bioverfügbarkeit ist nach wie vor gering (Berichten zufolge etwa 0,4-1 %).
Was sind die Vorteile der oralen Verabreichung von GLP-1-Peptid-Liposomen?
Orale GLP-1-Peptid-Liposomen können die Patientenfreundlichkeit und die Therapietreue verbessern, indem sie Injektionen überflüssig machen und gleichzeitig die effektive Absorption erhöhen, indem sie die Peptide vor Säure- und Enzymabbau schützen und den Transport durch Schleim- und Epithelbarrieren verbessern. Eine verbesserte orale Bioverfügbarkeit kann die Dosisbelastung verringern, den Kostendruck senken und die Hemmschwelle für Patienten senken, eine langfristige Peptidtherapie zu beginnen und beizubehalten.

Hielscher Ultrasonics fertigt Hochleistungs-Ultraschall-Homogenisatoren vom Labor bis zum voll-kommerziellen Industriemaßstab.



