Liposomales Semaglutid könnte der nächste große Schritt bei der Verabreichung von GLP-1-Medikamenten sein
, Kathrin Hielscher, veröffentlicht in Hielscher News
GLP-1-Peptide wie Semaglutid haben sich in den letzten zehn Jahren zu einem der einflussreichsten Peptidtherapeutika entwickelt, das bei Typ-2-Diabetes und Adipositas breite klinische Anwendung findet. Doch trotz seines klinischen Erfolgs sind die Herausforderungen bei der Formulierung und Herstellung von Semaglutid nach wie vor repräsentativ für Peptidmedikamente im Allgemeinen: Sie sind strukturell fragil, schwer gegen Abbau zu schützen und bekanntermaßen schwer auf nicht-invasivem Weg zu verabreichen. Diese Einschränkungen sind ein wesentlicher Grund dafür, dass die meisten GLP-1-Rezeptor-Agonisten nach wie vor gespritzt werden müssen, auch wenn die Nachfrage nach oraler oder patientenfreundlicher Verabreichung weiter steigt.
Die Grenzen der derzeitigen oralen GLP-1-Formulierungen
Die Entwicklung oraler GLP-1-Peptide hat gezeigt, dass eine orale Verabreichung technisch möglich ist, aber sie hat auch die wesentlichen Grenzen der bestehenden Strategien aufgezeigt. Selbst in einem zugelassenen Produkt weist orales Semaglutid eine sehr geringe Bioverfügbarkeit auf, die in der Regel unter 1 % liegt, was eine höhere Dosierung erforderlich macht und zu Kosten, Variabilität und Komplexität der Formulierung beiträgt. Diese Einschränkungen haben das Interesse an trägerbasierten Systemen verstärkt, die Peptidmedikamente schützen und die Absorption potenziell verbessern können, ohne ausschließlich auf chemische Permeationsverstärker angewiesen zu sein.
Liposomen als technisch ausgereifte Verabreichungsplattform
 Unter den untersuchten Verabreichungssystemen zeichnet sich die liposomale Verkapselung durch ihre technische Reife und pharmazeutische Relevanz aus. Liposomen bestehen aus Phospholipid-Doppelschichten, die biologischen Membranen sehr ähnlich sind und seit langem klinisch in der Onkologie und bei Infektionskrankheiten eingesetzt werden. Ihre Bedeutung für Peptidtherapeutika liegt in ihrer Fähigkeit, empfindliche Wirkstoffe physikalisch zu schützen und gleichzeitig Größe, Zusammensetzung und Oberflächeneigenschaften zu verändern. Die Leistungsfähigkeit von Liposomen hängt jedoch stark von der Größenverteilung, der Struktur der Doppelschicht, der Beladungsstrategie und der Reproduzierbarkeit der Herstellung ab. – Faktoren, die in erster Linie durch die Prozesstechnologie und nicht allein durch die Zusammensetzung der Formulierung bestimmt werden.
Unter den untersuchten Verabreichungssystemen zeichnet sich die liposomale Verkapselung durch ihre technische Reife und pharmazeutische Relevanz aus. Liposomen bestehen aus Phospholipid-Doppelschichten, die biologischen Membranen sehr ähnlich sind und seit langem klinisch in der Onkologie und bei Infektionskrankheiten eingesetzt werden. Ihre Bedeutung für Peptidtherapeutika liegt in ihrer Fähigkeit, empfindliche Wirkstoffe physikalisch zu schützen und gleichzeitig Größe, Zusammensetzung und Oberflächeneigenschaften zu verändern. Die Leistungsfähigkeit von Liposomen hängt jedoch stark von der Größenverteilung, der Struktur der Doppelschicht, der Beladungsstrategie und der Reproduzierbarkeit der Herstellung ab. – Faktoren, die in erster Linie durch die Prozesstechnologie und nicht allein durch die Zusammensetzung der Formulierung bestimmt werden.
Warum die Ultraschallverarbeitung für die Liposomenherstellung von zentraler Bedeutung ist
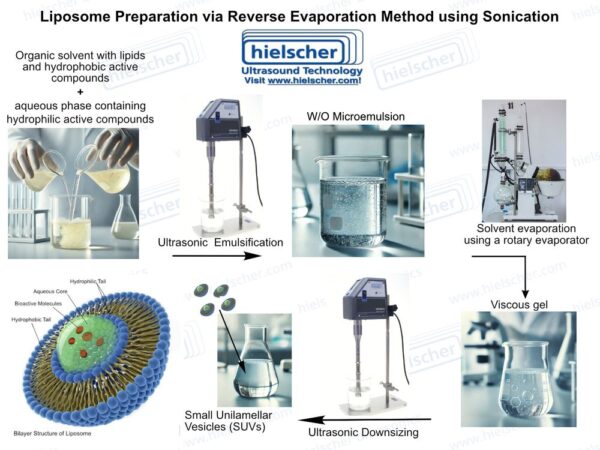
Die Ultraschallverarbeitung ist eine Antwort auf mehrere der zentralen Herausforderungen bei der Liposomenherstellung. Ultraschall mit hoher Intensität erzeugt akustische Kavitation in Flüssigkeiten, wodurch lokale Scherkräfte und Mikrovermischungseffekte entstehen, die Lipidaggregate aufbrechen und multilamellare Strukturen in kleinere, einheitlichere Vesikel umwandeln können. Bei der Liposomenherstellung kann Ultraschall während der Vesikelbildung oder als Nachbearbeitungsschritt eingesetzt werden, um die Partikelgröße und die Dispersionsqualität zu standardisieren. Diese Doppelrolle macht den Ultraschall besonders wertvoll für die Kontrolle kritischer Qualitätsmerkmale von Liposomensystemen.
Strukturelle Kompatibilität von Semaglutid mit Lipid-Doppelschichten
GLP-1-Peptide wie Semaglutid oder Tirzepatid eignen sich besonders gut für lipidbasierte Träger, da es sich nicht um ein einfaches lineares Peptid handelt. Das Molekül enthält einen chemisch modifizierten Lipidschwanz, der die Interaktion mit Lipidmembranen fördert. Experimentelle Studien mit Vesikelsystemen haben gezeigt, dass Semaglutid und verwandte Peptide durch Einfügung dieses Lipidschwanzes mit Vesikelmembranen assoziieren können. Obwohl diese Ergebnisse mit aus Milch gewonnenen extrazellulären Vesikeln und nicht mit synthetischen Liposomen erzielt wurden, ist der zugrunde liegende Mechanismus direkt übertragbar. Lipidierte Peptide haben eine inhärente Affinität für Phospholipid-Doppelschichten, was die Beladungseffizienz und Formulierungsstabilität verbessern kann, ohne dass eine komplexe chemische Konjugation erforderlich ist.
Prozessbedingungen bestimmen die Effizienz der Verkapselung
Eine wichtige Erkenntnis aus neueren Studien auf Vesikelbasis ist, dass die Verkapselungseffizienz in hohem Maße von der Beladungs- und Verarbeitungsmethode abhängt. Dies hat wichtige Auswirkungen auf die pharmazeutische Entwicklung: Der Erfolg oder Misserfolg einer Peptid-Liposomen-Formulierung hängt oft weniger von der Wahl des Lipids als vielmehr von der Art der Herstellung und Verarbeitung der Vesikel ab. Die Ultraschallverarbeitung bietet ein kontrollierbares und reproduzierbares Mittel zur Beeinflussung dieser Parameter, was sie für die systematische Formulierungsentwicklung besonders attraktiv macht.
Skalierbarkeit als Hauptvorteil der Ultraschallverarbeitung
Vom Standpunkt der Herstellung aus gesehen ist einer der wichtigsten Vorteile des Ultraschalls seine Skalierbarkeit. Im Gegensatz zu vielen Verfahren zur Herstellung von Nanopartikeln, die auf geometriespezifischen Batch-Bedingungen beruhen, lässt sich die Ultraschallverarbeitung durch Steuerung des Energieeintrags pro Volumeneinheit skalieren. Dadurch lassen sich im Labormaßstab entwickelte Prozesse mit hoher Vergleichbarkeit auf Pilot- und Industriesysteme übertragen. Für Pharmahersteller bedeutet dies Reproduzierbarkeit, Validierung und einen effizienten Technologietransfer über verschiedene Entwicklungsstufen hinweg.
Kontinuierliche Durchflussbeschallung für die industrielle Produktion
Die industriell relevanteste Anwendung der Ultraschall-Liposomenverarbeitung ist der Durchflussbetrieb. In Durchflussbeschallungszellen durchlaufen Liposomendispersionen ein definiertes Reaktorvolumen, während Ultraschall mit kontrolliertem Druck, Amplitude und Temperatur angewendet wird. Diese Konfiguration ermöglicht eine genaue Kontrolle der Verweilzeit und der Energieeinwirkung. Bei peptidbeladenen Liposomen, bei denen thermische Empfindlichkeit und strukturelle Integrität entscheidend sind, ist eine solche Kontrolle für die Aufrechterhaltung der Produktqualität in großem Maßstab unerlässlich.
Bedeutung für GLP-1- und Peptidtherapeutika der nächsten Generation
Da sich die GLP-1-Therapien in Richtung Dual- und Multi-Agonisten-Peptide weiterentwickeln, wird die Komplexität der Formulierung voraussichtlich zunehmen. Gleichzeitig wächst die Nachfrage der Patienten nach oralen oder weniger invasiven Verabreichungswegen. Skalierbare trägerbasierte Verabreichungsplattformen werden daher strategisch wichtig, nicht nur um die Pharmakokinetik zu verbessern, sondern auch um sicherzustellen, dass neue Peptidmedikamente zuverlässig im kommerziellen Maßstab hergestellt werden können.
Überwindung der grundlegenden Barriere bei der oralen Peptidverabreichung
Der Magen-Darm-Trakt ist von Natur aus feindselig gegenüber Peptiden, und die geringe orale Bioverfügbarkeit bleibt selbst für fortschrittliche Formulierungen ein grundlegendes Hindernis. Die liposomale Verkapselung beseitigt diese Herausforderung nicht, aber sie bietet einen rationalen technischen Ansatz zur Verringerung des Abbaus und zur Kontrolle der Interaktion von Peptiden mit der Darmumgebung. In Kombination mit skalierbaren Verarbeitungstechnologien wie Ultraschall nähern sich liposomenbasierte Verabreichungssysteme der industriellen Machbarkeit an, anstatt auf Laborversuche beschränkt zu bleiben.
Von der Laborentwicklung zur industriellen Umsetzung
 In praktischen Entwicklungsabläufen werden Hielscher Ultrasonics-Systeme häufig als Referenzplattform für die Ultraschall-Liposomenverarbeitung eingesetzt. Im Labor- und Formulierungsentwicklungsmaßstab ermöglichen kompakte Ultraschallsonden wie die UP200Ht und UP400St eine kontrollierte Kleinchargenverarbeitung und Methodenoptimierung. Für die industrielle Fertigung unterstützen Sonicators mit Durchflussreaktoren einen kontinuierlichen Betrieb, eine hohe Leistungsdichte und ein lineares Scale-up. Diese Eigenschaften entsprechen den Anforderungen der pharmazeutischen Produktion, einschließlich Prozesskontrolle und Reproduzierbarkeit.
In praktischen Entwicklungsabläufen werden Hielscher Ultrasonics-Systeme häufig als Referenzplattform für die Ultraschall-Liposomenverarbeitung eingesetzt. Im Labor- und Formulierungsentwicklungsmaßstab ermöglichen kompakte Ultraschallsonden wie die UP200Ht und UP400St eine kontrollierte Kleinchargenverarbeitung und Methodenoptimierung. Für die industrielle Fertigung unterstützen Sonicators mit Durchflussreaktoren einen kontinuierlichen Betrieb, eine hohe Leistungsdichte und ein lineares Scale-up. Diese Eigenschaften entsprechen den Anforderungen der pharmazeutischen Produktion, einschließlich Prozesskontrolle und Reproduzierbarkeit.
Jenseits von Semaglutid: Eine Plattform-Perspektive
Semaglutid dient zwar als äußerst relevante Modellverbindung, doch die Auswirkungen der Ultraschall-Liposomenverkapselung gehen über einen einzelnen Wirkstoff hinaus. Die gleiche Prozesslogik gilt für andere lipidierte Peptide, Peptidkonjugate und neue Biologika. Mit der zunehmenden Verbreitung von Peptidtherapeutika in den Bereichen Stoffwechselkrankheiten, Onkologie und Immunologie werden skalierbare Verkapselungstechnologien wahrscheinlich zu entscheidenden Faktoren dafür, welche Verabreichungsstrategien vom Konzept zur kommerziellen Realität werden können.
Der Wandel hin zu einer prozessgesteuerten Peptidabgabe
Ultraschall-verkapseltes liposomales Semaglutid veranschaulicht eine breitere Verlagerung in der pharmazeutischen Entwicklung: von Formulierungskonzepten, die in erster Linie auf biologischen Überlegungen beruhen, hin zu Verabreichungssystemen, die auf Verfahrenstechnik und Herstellbarkeit basieren. In einem Bereich, in dem viele orale Peptidtechnologien beim Scale-up scheitern, bietet die Ultraschall-Liposomenverarbeitung einen vergleichsweise direkten und technisch robusten Weg von der Laborentwicklung zur industriellen Produktion.
Literatur / Literaturhinweise
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
Häufig gestellte Fragen
Was sind GLP-1-Peptide?
GLP-1-Peptide sind Inkretin-mimetische Peptidmedikamente, die den Glucagon-like Peptide-1-Rezeptor (GLP-1R) aktivieren, einen Schlüsselrezeptor des Stoffwechsels, der an der glukoseabhängigen Insulinsekretion, der Unterdrückung der Glucagonfreisetzung, der verzögerten Magenentleerung und der Appetitregulierung beteiligt ist. Klinisch verwendete GLP-1-Peptide (wie Semaglutid) sind chemisch modifiziert, um dem enzymatischen Abbau zu widerstehen und eine längere Zirkulationszeit als natives GLP-1 zu erreichen.
Was ist der Unterschied zwischen Semaglutid und Tirzepatid?
Semaglutid ist ein Single-Agonist, der selektiv den Glucagon-like Peptide-1-Rezeptor (GLP-1R) aktiviert, während Tirzepatid ein dualer Agonist ist, der sowohl den GLP-1-Rezeptor als auch den Rezeptor für glukoseabhängiges insulinotropes Polypeptid (GIPR) aktiviert. Biochemisch gesehen ist Tirzepatid ein größeres und komplexeres Peptid mit Sequenzelementen und rezeptorbindenden Domänen, die für die Aktivierung von zwei Inkretinrezeptoren optimiert sind, während Semaglutid speziell für die hochaffine Aktivierung des GLP-1R entwickelt wurde. Beide Peptide sind chemisch mit Lipidbestandteilen modifiziert, um die Plasmaproteinbindung zu erhöhen und die systemische Halbwertszeit zu verlängern, aber die Doppelrezeptoraktivität von Tirzepatid führt zu einer breiteren metabolischen Signalwirkung.
Wie werden Semaglutid und Tirzepatid biochemisch klassifiziert?
Semaglutid wird biochemisch als lang wirkendes, lipidiertes GLP-1-Rezeptor-Agonistenpeptid eingestuft. Tirzepatid wird als langwirksamer, lipidierter dualer Inkretinrezeptor-Agonist eingestuft, insbesondere als GLP-1R/GIPR-Koagonist.

Hielscher Ultrasonics fertigt Hochleistungs-Ultraschall-Homogenisatoren vom Labor bis zum voll-kommerziellen Industriemaßstab.