인단백체학을 위한 초음파 처리 보조 단백질 추출
현대 생명과학에서 인산화단백체학은 세포 신호 경로를 해독하고 시스템 수준에서 질병 메커니즘을 이해하기 위한 초석 기술로 부상했습니다. 인산화는 중요한 생물학적 기능을 지배하기 때문입니다. – 효소 활성부터 단백질-단백질 상호작용까지 – 정밀한 측정은 기초 연구와 중개 의학 모두에 필수적입니다. 최근 질량 분석법의 발전으로 단일 실험에서 수만 개의 인산화 이벤트를 식별할 수 있게 되면서 강력하고 확장 가능하며 재현 가능한 샘플 준비 워크플로우의 필요성이 강조되고 있습니다.
이 분야에서 가장 영향력 있는 발전 중 하나는 시료 품질, 처리량 및 재현성을 크게 향상시키는 초음파 처리 보조 단백질 추출의 채택입니다. 특히 처리량이 많은 포스포프로테오믹스 분야에서 VialTweeter 및 UIP400MTP와 같은 초음파 기술은 이제 실험실에서 대규모 샘플 코호트를 처리하는 방법을 재정의하고 있습니다.
인산화단백체학에서 효율적인 시료 준비의 과학적 중요성
 단백질 인산화는 인간 세포의 대부분의 단백질에 영향을 미치는 매우 역동적이고 가역적인 번역 후 변형입니다. 단백질 구조, 위치 및 상호 작용 네트워크를 조절하며, 조절 장애는 암 및 신경 퇴화와 같은 질병과 관련이 있습니다.
단백질 인산화는 인간 세포의 대부분의 단백질에 영향을 미치는 매우 역동적이고 가역적인 번역 후 변형입니다. 단백질 구조, 위치 및 상호 작용 네트워크를 조절하며, 조절 장애는 암 및 신경 퇴화와 같은 질병과 관련이 있습니다.
그러나 인산화 단백질체 분석은 고유한 기술적 과제를 안고 있습니다. 인산화 펩타이드는 종종 그 양이 적기 때문에 신중한 농축과 매우 효율적인 업스트림 샘플 준비가 필요합니다. 단백질 추출 또는 소화 과정에서 비효율성이 발생하면 신호 손실, 재현성 저하, 불완전한 인산화 범위로 이어질 수 있습니다.
바로 이때 초음파 처리가 중요해집니다.

40개의 오토샘플러 바이알 초음파 처리 단백질 추출을 위한 UIP400MTP로
초음파 처리가 단백질 추출을 혁신하는 이유
초음파 처리는 고강도 초음파를 사용하여 세포와 조직을 기계적으로 파괴하여 세포, 조직, 생체액 및 세포 외 소포에서 단백질을 효율적으로 방출할 수 있습니다. 기존의 용해 기술과 비교할 때 초음파 처리는 몇 가지 뚜렷한 이점을 제공합니다:
- 첫째, 신속하고 균일한 세포 파괴를 보장하며, 이는 일시적인 인산화 상태를 보존하는 데 특히 중요합니다. 인산화단백체학에서는 약간의 지연이나 불완전한 용해로도 신호 프로필이 변경될 수 있으므로 빠르고 재현 가능한 추출이 필수적입니다.
- 둘째, 초음파 처리는 특히 치밀한 조직이나 막이 풍부한 세포와 같이 분해하기 어려운 시료의 단백질 수율과 가용화를 개선합니다. 이는 곧 더 나은 다운스트림 소화 및 포스포펩타이드 회수로 직결됩니다.
- 셋째, 초음파 처리는 본질적으로 확장성이 뛰어납니다. 바이알트위터와 같은 장치를 사용하면 여러 개의 밀봉된 튜브를 동시에 초음파 처리할 수 있으므로 시료 전반에 걸쳐 동일한 처리 조건을 보장할 수 있습니다. 따라서 수동 처리로 인한 변동성이 제거됩니다.
- 더 높은 처리량이 요구되는 경우, UIP400MTP는 중요한 기술적 도약을 의미합니다. 자동 샘플러 바이알을 포함하여 전체 마이크로플레이트 또는 튜브 랙을 직접 초음파 처리할 수 있어 수백 개의 샘플을 병렬로 처리하는 데 이상적입니다. 이 기능은 대규모 샘플 코호트가 표준인 시스템 생물학 및 임상 연구에서 특히 유용합니다.

바이알트위터: 제어된 공정 파라미터에서 여러 시료의 동시 초음파 처리
고처리량 초음파 처리: 바이알트위터와 UIP400MTP의 집중 조명
고급 초음파 장치를 인산화단백질 워크플로우에 통합하는 것은 단순히 편리함만을 위한 것이 아닙니다. – 방법론적인 개선입니다.
바이알트위터는 여러 개의 밀폐된 바이알을 동시에 초음파 처리하도록 설계되어 교차 오염을 최소화하는 동시에 재현성을 보장합니다. 특히 중간 처리량 애플리케이션과 표준화된 워크플로우에 적합합니다.
반면 UIP400MTP는 처리량이 많은 환경에 최적화되어 있습니다:
- 전체 표준 마이크로 플레이트(예: 96웰 또는 384웰 플레이트)에서 균일한 초음파 처리
- 튜브 랙 및 자동 샘플러 바이알의 직접 처리
- 실습 시간 대폭 단축
- 대규모 데이터 세트의 재현성 향상
이러한 확장성은 워크플로우가 일상적으로 수십에서 수백 개의 샘플을 병렬로 처리하는 최신 인산화단백체학 접근 방식에 완벽하게 부합합니다.
초음파 처리 보조 인산화단백질 시료 준비를 위한 일반 프로토콜
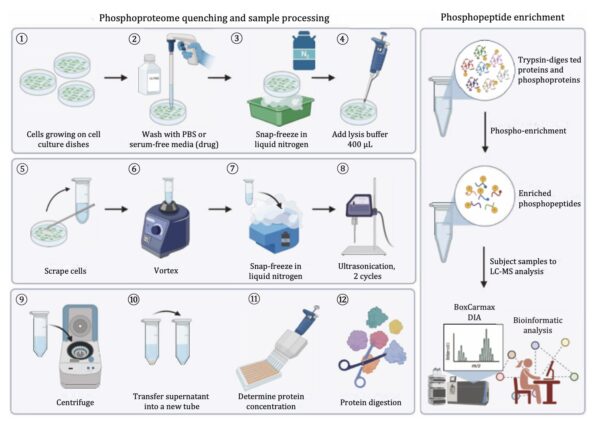
강력한 포스포프로테오믹스 워크플로우는 효율적인 단백질 추출, 효소 분해 및 포스포펩타이드 농축을 통합합니다. 다음 개요는 초음파 처리 기반 준비에 적합한 확립된 모범 사례를 반영합니다:
- 신속한 시료 담금질 및 수집
세포 또는 조직이 빠르게 소멸됩니다. – 일반적으로 스냅 프리징을 통해 – 를 사용하여 인산화 상태를 보존합니다. 이 단계는 인산화 이벤트의 일시적인 특성으로 인해 매우 중요합니다. - 초음파 세포 용해 및 단백질 추출
샘플을 해동하고 일반적으로 짧은 주기로 초음파 처리를 합니다. 초음파 에너지는 세포막을 파괴하고 단백질을 효율적으로 방출합니다. 검증된 워크플로에서는 초음파 처리를 여러 주기로 수행하여 완전한 용해를 보장합니다.
예시: 샘플을 얼음에서 해동한 후, Vialtweeter 기기와 같은 초음파 처리기를 사용하여 각 사이클 1분씩 2사이클 동안 세포 용해를 수행했습니다. - 설명 및 단백질 정량화
용해 후 샘플을 원심분리하여 이물질을 제거합니다. 용해성 단백질이 포함된 상청액을 수집하고 정량화하여 샘플 전체에 걸쳐 일관성 있는 결과를 얻을 수 있도록 합니다. - 환원 및 알킬화
이황화 결합을 감소(예: DTT 사용)하고 알킬화(예: IAA 사용)하여 단백질을 안정화하고 소화 효율을 개선합니다. - 단백질 분해 소화(proteolytic digestion)
단백질은 일반적으로 트립신으로 효소 분해되어 질량 분석에 적합한 펩타이드를 생성합니다. 초음파 가속 단백질 소화에 대해 자세히 알아보세요! - 펩타이드 정제 및 탈염
펩타이드는 LC-MS 분석을 방해할 수 있는 오염 물질을 제거하기 위해 C18 기반 방법을 사용하여 정제합니다. - 포스포펩타이드 농축
인산화 펩타이드의 농도가 낮기 때문에 인산화 펩타이드를 선택적으로 분리하기 위해 Fe-NTA 또는 TiO₂ 친화성 방법과 같은 농축 기법을 적용합니다. - LC-MS/MS 분석 및 데이터 처리
농축 샘플은 고해상도 질량 분석법을 사용하여 분석하며, 정량화 및 재현성을 개선하기 위해 데이터 독립적 수집(DIA)을 사용하는 경우가 많습니다.
특히 대규모 워크플로를 96웰 플레이트 형식에 맞게 조정할 수 있어 최대 수백 개의 샘플을 병렬 처리할 수 있습니다. – UIP400MTP 기반 초음파 처리와 완벽하게 호환되는 접근 방식입니다.
초음파 처리를 통한 재현성 및 데이터 품질 향상
포스포프로테오믹스의 핵심 과제 중 하나는 대규모 데이터 세트에서 일관된 정량화를 달성하는 것입니다. 샘플 준비 과정에서 발생하는 변수는 생물학적으로 의미 있는 차이를 모호하게 만들 수 있습니다.
초음파 처리를 통해 이 문제를 해결합니다:
- 샘플 전반에 걸쳐 표준화된 에너지 입력
- 수동 변동성 감소
- 단백질 추출 및 소화의 재현성 향상
UIP400MTP와 같은 고처리량 플랫폼과 결합하면 실험실은 시스템 생물학 연구와 임상 바이오마커 발견에 필수적인 수준의 일관성을 달성할 수 있습니다.
포스포프로테오믹스의 미래: 자동화 및 확장성
포스포프로테오믹스가 대규모 임상 응용 분야로 계속 확장됨에 따라 자동화 및 처리량에 대한 수요는 더욱 증가할 것입니다. 특히 마이크로플레이트 호환 시스템과 통합된 초음파 처리 기반 샘플 준비는 이를 가능하게 하는 핵심 기술입니다.
효율적인 초음파 용해, 병렬 처리, 자동화된 워크플로와의 호환성을 결합하여 VialTweeter 및 UIP400MTP와 같은 장치는 단백질학 샘플 준비의 새로운 표준을 제시하고 있습니다.
자동화된 실험실 워크플로우에 UIP400MTP를 통합하는 방법에 대해 자세히 알아보세요!
인산화 단백체학에서 초음파 처리 보조 샘플 준비의 이점을 활용하세요!
초음파를 이용한 단백질 추출은 탁월한 효율성, 확장성 및 재현성을 제공하는 현대 인산화단백체학의 핵심 구성 요소로 자리 잡았습니다. 대규모 샘플 코호트에서 복잡한 생물학적 시스템을 분석해야 할 필요성이 증가함에 따라 초음파 기술은 단순히 유리한 것만이 아닙니다. – 필수적인 요소입니다.
높은 처리량의 표준화된 워크플로우를 지원하는 VialTweeter 및 UIP400MTP와 같은 솔루션은 세포 신호, 질병 메커니즘 및 정밀 의학 분야의 발견을 가속화하고 있습니다.
설계, 제조 및 컨설팅 – 독일에서 만든 품질
Hielscher 초음파는 최고의 품질과 디자인 표준으로 잘 알려져 있습니다. 견고 함과 쉬운 작동으로 초음파를 산업 시설에 원활하게 통합 할 수 있습니다. 거친 조건과 까다로운 환경은 Hielscher 초음파기로 쉽게 처리 할 수 있습니다.
Hielscher 초음파는 ISO 인증 회사이며 최첨단 기술과 사용자 친화성을 갖춘 고성능 초음파에 특히 중점을 둡니다. 물론, Hielscher 초음파는 CE를 준수하며 UL, CSA 및 RoHs의 요구 사항을 충족합니다.
자주 묻는 질문
포스포프로테오믹스란 무엇인가요?
인산화단백체학은 단백질 인산화 부위의 대규모 식별, 국소화 및 정량화에 초점을 맞춘 단백질체학의 전문 분야입니다. 인산화 단백질과 펩타이드를 분석하여 단백질 기능을 제어하는 세포 신호 경로, 조절 메커니즘, 번역 후 동적 변형을 이해합니다.
인산화 확인이 어려운 이유는 무엇인가요?
인산화 이벤트는 종종 일시적이고, 그 양이 적으며, 화학량론이 낮은 상태에서 발생하기 때문에 인산화를 확인하기가 어렵습니다. 또한 인산화 펩타이드는 화학적 불안정성, 질량 분석의 이온화 변동성, 펩타이드 서열 내에서 인산화 부위를 정확하게 할당하는 복잡성으로 인해 검출하기 어려울 수 있습니다.
인단백질이란 무엇인가요?
인산화 단백질은 인산화 과정을 거친 단백질로, 하나 이상의 인산염기가 특정 아미노산 잔기(일반적으로 세린, 트레오닌 또는 티로신)에 공유 결합된 것을 의미합니다. 이러한 변형은 단백질의 활성, 구조, 위치 또는 다른 분자와의 상호 작용을 변경할 수 있습니다.
프로테오믹스와 인산화단백체학의 차이점은 무엇인가요?
단백질체학은 생물학적 시스템에서 발현되는 모든 단백질의 풍부함, 구조, 상호작용을 포함한 포괄적인 연구입니다. 반면 인산화단백체학은 인산화되는 단백질의 하위 집합에 초점을 맞추고 인산화 부위와 세포 과정에서의 조절 역할에 대한 분석을 강조합니다.
문헌 / 참고문헌
- FactSheet UIP400MTP Plate-Sonicator for High-Throughput Sample Preparation – English version – Hielscher Ultrasonics
- FactSheet VialTweeter – Sonicator for Simultaneous Sample Preparation
- FactSheet UIP400MTP Plate-Sonicator für die High-Throughput Probenvorbereitung in 96-Well-Platten – deutsch – Hielscher Ultrasonics
- Di Y, Li W, Salovska B, Ba Q, Hu Z, Wang S, Liu Y. (2023): A basic phosphoproteomic-DIA workflow integrating precise quantification of phosphosites in systems biology. Biophysics Reports. 2023 Apr 30;9(2):82-98.
- Cosenza-Contreras M, Seredynska A, Vogele D, Pinter N, Brombacher E, Cueto RF, Dinh TJ, Bernhard P, Rogg M, Liu J, Willems P, Stael S, Huesgen PF, Kuehn EW, Kreutz C, Schell C, Schilling O. (2024): TermineR: Extracting information on endogenous proteolytic processing from shotgun proteomics data. Proteomics. 2024.
- Gao, Erli; Li, Wenxue; Wu, Chongde; Shao, Wenguang; di, Yi; Liu, Yansheng (2021): Data-independent Acquisition-based Proteome and Phosphoproteome Profiling across Six Melanoma Cell Lines Reveals Determinants of Proteotypes. Molecular Omics. 2021