リポソームセマグルチドはGLP-1薬物送達における次の飛躍的進歩の可能性
, カトリーン・ヒールシャーHielscher Newsに掲載
セマグルチドに代表されるGLP-1ペプチドは、2型糖尿病や肥満症に広く臨床応用され、過去10年間で最も影響力のあるペプチド治療薬のひとつとなった。しかし、その臨床的成功にもかかわらず、セマグルチドの製剤学的・製造学的課題は、一般的なペプチド医薬品を代表するものであることに変わりはない。このような限界は、経口投与や患者に優しい投与方法への需要が高まり続けているにもかかわらず、ほとんどのGLP-1受容体作動薬がいまだに注射に頼っている主な理由である。
現在の経口GLP-1製剤の限界
経口GLP-1ペプチドの開発は、経口投与が技術的に可能であることを示したが、同時に既存の戦略の核心的な限界も露呈した。承認された製品であっても、経口セマグルチドのバイオアベイラビリティは非常に低く、通常1%以下であるため、高用量投与が必要となり、コスト、ばらつき、製剤の複雑さの一因となっている。このような制約から、化学的浸透促進剤だけに頼ることなく、ペプチド医薬品を保護し、吸収を改善する可能性のある担体ベースのシステムへの関心が高まっている。
技術的に成熟した送達プラットフォームとしてのリポソーム
 現在研究されているデリバリー・システムの中で、リポソーム・カプセル化は、その技術的成熟度と薬学的妥当性において際立っている。リポソームは生体膜によく似たリン脂質二重膜で構成され、腫瘍学や感染症において臨床的に使用されてきた長い歴史がある。ペプチド治療薬との関連性は、サイズ、組成、表面特性を調整できる一方で、高感度な原薬を物理的に保護できる点にある。しかしながら、リポソームの性能は、サイズ分布、二重層構造、負荷戦略、製造の再現性に強く依存する。 – 製剤の組成だけでなく、主にプロセス技術に支配される要因である。
現在研究されているデリバリー・システムの中で、リポソーム・カプセル化は、その技術的成熟度と薬学的妥当性において際立っている。リポソームは生体膜によく似たリン脂質二重膜で構成され、腫瘍学や感染症において臨床的に使用されてきた長い歴史がある。ペプチド治療薬との関連性は、サイズ、組成、表面特性を調整できる一方で、高感度な原薬を物理的に保護できる点にある。しかしながら、リポソームの性能は、サイズ分布、二重層構造、負荷戦略、製造の再現性に強く依存する。 – 製剤の組成だけでなく、主にプロセス技術に支配される要因である。
超音波処理がリポソーム製造の中心である理由
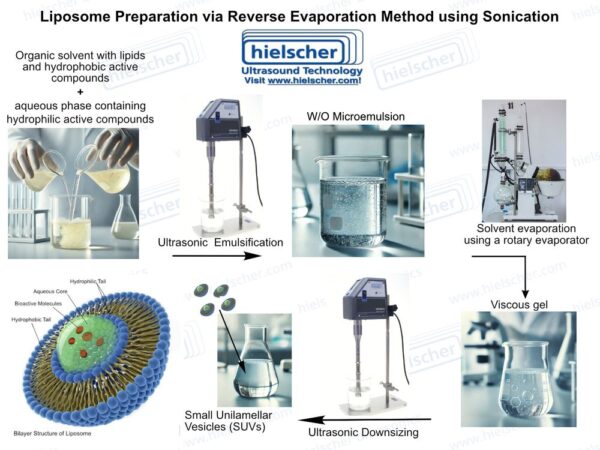
超音波処理は、リポソーム製造に関連するいくつかの主要な課題に対処する。高強度の超音波は液体中に音響キャビテーションを発生させ、局所的なせん断力とマイクロミキシング効果を生じさせ、脂質の凝集体を破壊し、多層構造をより小さく均一なベシクルに変換することができる。リポソーム製造において、超音波はベシクル形成中、または粒子径と分散品質を標準化するための後処理段階として適用することができる。この2つの役割により、超音波はリポソームシステムの重要な品質特性を制御する上で特に有用です。
セマグルチドと脂質二重膜の構造適合性
セマグルチドやティルゼパチドのようなGLP-1ペプチドは、単純な直鎖ペプチドではないので、脂質ベースのキャリアに特に適している。この分子には、脂質膜との相互作用を促進する化学修飾された脂質テールがある。小胞システムを用いた実験的研究から、セマグルチドや関連ペプチドはこの脂質テールの挿入によって小胞膜と会合できることが示されている。これらの知見は合成リポソームではなく、乳由来の細胞外小胞を用いて得られたものであるが、基本的なメカニズムはそのまま転用可能である。脂質化ペプチドはリン脂質二重膜に対して固有の親和性を持っており、複雑な化学的コンジュゲーションを必要とすることなく、ローディング効率と製剤安定性を向上させることができる。
プロセス条件がカプセル化効率を決定する
最近のベシクルを用いた研究から得られた重要な洞察は、カプセル化の効率が担持と処理方法に大きく依存するということである。これは医薬品開発にとって重要な意味を持つ。ペプチドリポソーム製剤の成否は、多くの場合、脂質の選択よりも、ベシクルの製造方法と処理方法に依存する。超音波処理は、これらのパラメーターに影響を与える制御可能で再現性のある手段を提供するため、系統的な製剤開発には特に魅力的である。
超音波処理の主な利点としてのスケーラビリティ
製造の観点から見ると、超音波の最も重要な利点の一つは、そのスケーラビリティである。形状固有のバッチ条件に依存する多くのナノ粒子製造技術とは異なり、超音波処理は単位体積当たりのエネルギー入力を制御することでスケールアップできる。このため、実験室規模で開発されたプロセスを、高い比較可能性でパイロット・システムや工業用システムに移行することができる。製薬メーカーにとって、この特性は再現性、バリデーション、開発段階を超えた効率的な技術移転をサポートする。
工業生産のための連続フローソニケーション
超音波リポソーム処理の最も工業的な実施方法は、連続フロー操作である。フロースルー超音波処理セルでは、リポソーム分散液は、圧力、振幅、温度を制御しながら超音波を印加しながら、決められたリアクター容積を通過します。この構成により、滞留時間とエネルギー照射を正確に制御することができる。熱感受性と構造的完全性が重要なペプチド負荷リポソームにとって、このような制御はスケールアップした製品の品質を維持するために不可欠です。
次世代GLP-1およびペプチド治療薬との関連性
GLP-1治療薬がデュアルアゴニストやマルチアゴニストペプチドへと進化するにつれて、製剤の複雑さが増すことが予想される。同時に、経口または侵襲性の低いデリバリールートに対する患者の要望も高まり続けている。したがって、スケーラブルなキャリアベースのデリバリー・プラットフォームは、薬物動態を改善するためだけでなく、新しいペプチド医薬品を商業規模で確実に製造するためにも、戦略的に重要になる。
経口ペプチドデリバリーの基本的障壁に対処する
消化管はペプチドに対して本質的に敵対的であり、経口バイオアベイラビリティの低さは、高度な製剤であっても依然として基本的な障壁である。リポソームカプセル化によってこの課題がなくなるわけではないが、分解を抑え、ペプチドが腸内環境とどのように相互作用するかをコントロールする合理的な工学的アプローチを提供する。超音波のようなスケーラブルな処理技術と組み合わせることで、リポソームベースのデリバリーシステムは、実験室での実験にとどまることなく、産業的な実現可能性に近づいていく。
研究室での開発から産業への導入へ
 実用的な開発ワークフローにおいて、ヒールシャー・ウルトラソニックス社のシステムは超音波リポソーム処理のリファレンス・プラットフォームとして頻繁に使用されています。実験室や製剤開発スケールでは、UP200HtやUP400Stのようなコンパクトな超音波プローブが、制御された少量バッチ処理とメソッドの最適化を可能にします。工業生産では、フロースルー反応器を備えた超音波プローブが、連続運転、高出力密度、リニアなスケールアップをサポートします。これらの特性は、プロセス制御や再現性など、医薬品製造環境の要件に合致しています。
実用的な開発ワークフローにおいて、ヒールシャー・ウルトラソニックス社のシステムは超音波リポソーム処理のリファレンス・プラットフォームとして頻繁に使用されています。実験室や製剤開発スケールでは、UP200HtやUP400Stのようなコンパクトな超音波プローブが、制御された少量バッチ処理とメソッドの最適化を可能にします。工業生産では、フロースルー反応器を備えた超音波プローブが、連続運転、高出力密度、リニアなスケールアップをサポートします。これらの特性は、プロセス制御や再現性など、医薬品製造環境の要件に合致しています。
セマグルチドを超えてプラットフォームの視点
セマグルチドは非常に関連性の高いモデル化合物であるが、超音波リポソームカプセル化の意義は単一の原薬にとどまらない。同じプロセスロジックが、他の脂質化ペプチド、ペプチド結合体、新興の生物製剤にも適用される。ペプチド治療薬が代謝性疾患、腫瘍学、免疫学に拡大するにつれて、スケーラブルなカプセル化技術は、どのデリバリー戦略がコンセプトから商業的な現実へと進展するかを決定する決定的な要因となる可能性が高い。
プロセス工学的ペプチド送達へのシフト
超音波カプセル化リポソームセマグルチドは、製薬開発におけるより広範なシフトを示している。すなわち、主に生物学的合理性によって駆動される製剤コンセプトから、プロセス工学と製造可能性に根ざした送達システムへとシフトしている。多くの経口ペプチド技術がスケールアップ中に失敗するこの分野において、超音波リポソーム処理は、実験室での開発から工業生産への比較的直接的で技術的に強固な経路を提供する。
文献・参考文献
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
よくある質問
GLP-1ペプチドとは何か?
GLP-1ペプチドは、グルコース依存性インスリン分泌、グルカゴン放出抑制、胃排出遅延、食欲調節に関与する重要な代謝受容体であるグルカゴン様ペプチド-1受容体(GLP-1R)を活性化するインクレチン様ペプチド薬である。臨床的に使用されるGLP-1ペプチド(セマグルチドなど)は、酵素分解に抵抗し、ネイティブGLP-1と比較して循環時間を延長するために化学修飾されている。
セマグルチドとティルゼパチドの違いは?
セマグルチドはグルカゴン様ペプチド-1受容体(GLP-1R)を選択的に活性化するシングルアゴニストペプチドであり、ティルゼパチドはGLP-1受容体とグルコース依存性インスリン分泌刺激性ポリペプチド受容体(GIPR)の両方を活性化するデュアルアゴニストである。生化学的には、ティルゼパチドはより大きく複雑なペプチドで、配列要素や受容体結合ドメインが2つのインクレチン受容体に関与するように最適化されているのに対し、セマグルチドは高親和性GLP-1R活性化のために特別に設計されている。どちらのペプチドも、血漿タンパク質との結合を高め、全身的な半減期を延長するために、脂質部分で化学修飾されているが、tirzepatideの二重受容体活性は、より広範な代謝シグナル伝達をもたらす。
セマグルチドとティルゼパチドは生物化学的にどのように分類されるか?
セマグルチドは生化学的には長時間作用型の脂質化GLP-1受容体作動薬ペプチドに分類される。Tirzepatideは、長時間作用型の脂質化デュアルインクレチン受容体アゴニストペプチド、特にGLP-1R/GIPRコアゴニストに分類される。