Liposomal semaglutid kan være det næste store spring inden for GLP-1-lægemiddeltilførsel
, Kathrin Hielscher, udgivet i Hielscher News
GLP-1-peptider som semaglutid er blevet et af de mest indflydelsesrige peptidlægemidler i det sidste årti med bred klinisk anvendelse til behandling af type 2-diabetes og fedme. Men på trods af den kliniske succes er formulerings- og produktionsudfordringerne ved semaglutid stadig repræsentative for peptidlægemidler generelt: De er strukturelt skrøbelige, vanskelige at beskytte mod nedbrydning og notorisk svære at levere via ikke-invasive ruter. Disse begrænsninger er en væsentlig årsag til, at de fleste GLP-1-receptoragonister stadig er afhængige af indsprøjtninger, selv om efterspørgslen efter oral eller patientvenlig levering fortsætter med at vokse.
Grænser for nuværende orale GLP-1-formuleringer
Udviklingen af orale GLP-1-peptider viste, at oral levering er teknisk mulig, men den afslørede også de centrale begrænsninger i de eksisterende strategier. Selv i et godkendt produkt udviser oral semaglutid meget lav biotilgængelighed, typisk under 1 %, hvilket kræver højere dosering og bidrager til omkostninger, variabilitet og formuleringskompleksitet. Disse begrænsninger har intensiveret interessen for bærerbaserede systemer, der kan beskytte peptidlægemidler og potentielt forbedre absorptionen uden udelukkende at være afhængig af kemiske permeationsforstærkere.
Liposomer som en teknisk moden leveringsplatform
 Blandt de leveringssystemer, der undersøges, skiller liposomal indkapsling sig ud på grund af sin tekniske modenhed og farmaceutiske relevans. Liposomer består af fosfolipid-dobbeltlag, der minder meget om biologiske membraner og har en lang historie med klinisk brug inden for onkologi og infektionssygdomme. Deres relevans for peptidterapi ligger i deres evne til fysisk at beskytte følsomme API'er, samtidig med at de kan tilpasses i størrelse, sammensætning og overfladeegenskaber. Liposomernes ydeevne er dog stærkt afhængig af størrelsesfordeling, dobbeltlagsstruktur, indlæsningsstrategi og fremstillingens reproducerbarhed. – faktorer, der primært styres af procesteknologi snarere end formuleringens sammensætning alene.
Blandt de leveringssystemer, der undersøges, skiller liposomal indkapsling sig ud på grund af sin tekniske modenhed og farmaceutiske relevans. Liposomer består af fosfolipid-dobbeltlag, der minder meget om biologiske membraner og har en lang historie med klinisk brug inden for onkologi og infektionssygdomme. Deres relevans for peptidterapi ligger i deres evne til fysisk at beskytte følsomme API'er, samtidig med at de kan tilpasses i størrelse, sammensætning og overfladeegenskaber. Liposomernes ydeevne er dog stærkt afhængig af størrelsesfordeling, dobbeltlagsstruktur, indlæsningsstrategi og fremstillingens reproducerbarhed. – faktorer, der primært styres af procesteknologi snarere end formuleringens sammensætning alene.
Hvorfor ultralydsbehandling er central for liposomfremstilling
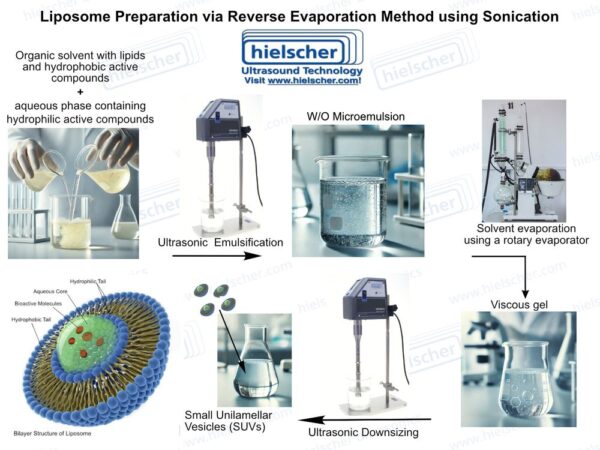
Ultralydsbehandling løser flere af de centrale udfordringer i forbindelse med liposomproduktion. Højintensiv ultralyd genererer akustisk kavitation i væsker, der producerer lokaliserede forskydningskræfter og mikroblandingseffekter, der kan nedbryde lipidaggregater og konvertere multilamellære strukturer til mindre, mere ensartede vesikler. I liposomfremstilling kan ultralyd anvendes under vesikeldannelse eller som et efterbehandlingstrin for at standardisere partikelstørrelse og dispersionskvalitet. Denne dobbelte rolle gør ultralyd særlig værdifuld til at kontrollere kritiske kvalitetsattributter for liposomale systemer.
Semaglutids strukturelle kompatibilitet med lipid-dobbeltlagre
GLP-1-peptider som semaglutid eller tirzepatid er særligt velegnede til lipidbaserede bærere, fordi det ikke er et simpelt lineært peptid. Molekylet indeholder en kemisk modificeret lipidhale, der fremmer interaktion med lipidmembraner. Eksperimentelle undersøgelser med vesikelsystemer har vist, at semaglutid og beslægtede peptider kan knytte sig til vesikelmembraner gennem indsættelse af denne lipidhale. Selvom disse resultater blev opnået ved hjælp af ekstracellulære vesikler fra mælk i stedet for syntetiske liposomer, er den underliggende mekanisme direkte overførbar. Lipiderede peptider har en iboende affinitet for fosfolipid-dobbeltlag, hvilket kan forbedre indlæsningseffektiviteten og formuleringsstabiliteten uden at kræve kompleks kemisk konjugering.
Procesbetingelser bestemmer indkapslingseffektivitet
En vigtig indsigt fra de seneste vesikelbaserede studier er, at indkapslingseffektiviteten i høj grad afhænger af påfyldnings- og behandlingsmetoden. Dette har vigtige konsekvenser for den farmaceutiske udvikling: succes eller fiasko for en peptid liposom formulering afhænger ofte mindre af valget af lipid og mere af, hvordan vesiklerne produceres og behandles. Ultralydsbehandling giver et kontrollerbart og reproducerbart middel til at påvirke disse parametre, hvilket gør det særligt attraktivt for systematisk formuleringsudvikling.
Skalerbarhed som en vigtig fordel ved ultralydsbehandling
Fra et produktionssynspunkt er en af de mest betydningsfulde fordele ved ultralyd dens skalerbarhed. I modsætning til mange nanopartikelproduktionsteknikker, der er afhængige af geometrispecifikke batchbetingelser, kan ultralydsbehandling skaleres ved at kontrollere energiinput pr. volumenenhed. Dette gør det muligt at overføre processer, der er udviklet i laboratorieskala, til pilot- og industrisystemer med høj sammenlignelighed. For lægemiddelproducenter understøtter denne egenskab reproducerbarhed, validering og effektiv teknologioverførsel på tværs af udviklingsstadier.
Kontinuerlig flow-sonikering til industriel produktion
Den mest industrielt relevante implementering af ultralydsliposombehandling er kontinuerlig flowdrift. I gennemstrømningssonikeringsceller passerer liposomdispersioner gennem et defineret reaktorvolumen, mens ultralyd påføres under kontrolleret tryk, amplitude og temperatur. Denne konfiguration muliggør præcis kontrol over opholdstid og energieksponering. For peptidbelastede liposomer, hvor termisk følsomhed og strukturel integritet er kritisk, er en sådan kontrol afgørende for at opretholde produktkvaliteten i stor skala.
Relevans for næste generation af GLP-1 og peptidterapi
Efterhånden som GLP-1-behandlinger udvikler sig i retning af peptider med to eller flere agonister, forventes formuleringskompleksiteten at stige. Samtidig fortsætter patienternes efterspørgsel efter orale eller mindre invasive indgivelsesmetoder med at vokse. Skalerbare bærerbaserede leveringsplatforme bliver derfor strategisk vigtige, ikke kun for at forbedre farmakokinetikken, men også for at sikre, at nye peptidlægemidler kan fremstilles pålideligt i kommerciel skala.
Håndtering af den grundlæggende barriere for oral peptidlevering
Mavetarmkanalen er i sagens natur fjendtlig over for peptider, og lav oral biotilgængelighed er stadig en grundlæggende barriere, selv for avancerede formuleringer. Liposomal indkapsling eliminerer ikke denne udfordring, men det giver en rationel teknisk tilgang til at reducere nedbrydning og kontrollere, hvordan peptider interagerer med tarmmiljøer. Når det kombineres med skalerbare behandlingsteknologier som ultralyd, kommer liposombaserede leveringssystemer tættere på industriel gennemførlighed i stedet for at forblive begrænset til laboratorieeksperimenter.
Fra laboratorieudvikling til industriel implementering
 I praktiske udviklingsarbejdsgange bruges Hielscher Ultrasonics-systemer ofte som referenceplatforme til ultralydsliposombehandling. På laboratorie- og formuleringsudviklingsskala muliggør kompakte ultralydssonder som UP200Ht og UP400St kontrolleret behandling af små partier og metodeoptimering. Til industriel fremstilling understøtter sonikatorer udstyret med gennemstrømningsreaktorer kontinuerlig drift, høj effekttæthed og lineær opskalering. Disse egenskaber stemmer overens med kravene i farmaceutiske produktionsmiljøer, herunder proceskontrol og reproducerbarhed.
I praktiske udviklingsarbejdsgange bruges Hielscher Ultrasonics-systemer ofte som referenceplatforme til ultralydsliposombehandling. På laboratorie- og formuleringsudviklingsskala muliggør kompakte ultralydssonder som UP200Ht og UP400St kontrolleret behandling af små partier og metodeoptimering. Til industriel fremstilling understøtter sonikatorer udstyret med gennemstrømningsreaktorer kontinuerlig drift, høj effekttæthed og lineær opskalering. Disse egenskaber stemmer overens med kravene i farmaceutiske produktionsmiljøer, herunder proceskontrol og reproducerbarhed.
Ud over semaglutid: Et platformsperspektiv
Mens semaglutid fungerer som en meget relevant modelforbindelse, strækker konsekvenserne af ultralydsliposomindkapsling sig ud over en enkelt API. Den samme proceslogik gælder for andre lipiderede peptider, peptidkonjugater og nye biologiske lægemidler. Efterhånden som peptidterapier udvides på tværs af metaboliske sygdomme, onkologi og immunologi, vil skalerbare indkapslingsteknologier sandsynligvis blive afgørende faktorer for at bestemme, hvilke leveringsstrategier der kan gå fra koncept til kommerciel virkelighed.
Et skift mod procesudviklet peptidlevering
Ultralydsindkapslet liposomal semaglutid illustrerer et bredere skift i den farmaceutiske udvikling: fra formuleringskoncepter, der primært er drevet af biologisk rationale, til leveringssystemer, der er baseret på procesteknik og fremstillingsevne. I et felt, hvor mange orale peptidteknologier mislykkes under opskalering, tilbyder ultralydsliposombehandling en forholdsvis direkte og teknisk robust vej fra laboratorieudvikling til industriel produktion.
Litteratur / Referencer
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
Ofte stillede spørgsmål
Hvad er GLP-1-peptider?
GLP-1-peptider er inkretin-mimetiske peptidlægemidler, der aktiverer den glukagonlignende peptid-1-receptor (GLP-1R), en vigtig metabolisk receptor, der er involveret i glukoseafhængig insulinudskillelse, undertrykkelse af glukagonfrigivelse, forsinket mavetømning og appetitregulering. Klinisk anvendte GLP-1-peptider (såsom semaglutid) er kemisk modificerede for at modstå enzymatisk nedbrydning og for at opnå længere cirkulationstid sammenlignet med naturligt GLP-1.
Hvad er forskellen mellem Semaglutid og Tirzepatid?
Semaglutid er et peptid med én agonist, der selektivt aktiverer den glukagonlignende peptid-1-receptor (GLP-1R), mens tirzepatid er en dobbelt agonist, der aktiverer både GLP-1-receptoren og den glukoseafhængige insulinotropiske polypeptidreceptor (GIPR). Biokemisk set er tirzepatid et større og mere komplekst peptid med sekvenselementer og receptorbindende domæner, der er optimeret til at aktivere to inkretinreceptorer, mens semaglutid er udviklet specifikt til GLP-1R-aktivering med høj affinitet. Begge peptider er kemisk modificeret med lipiddele for at øge plasmaproteinbindingen og forlænge den systemiske halveringstid, men tirzepatids dobbeltreceptoraktivitet resulterer i en bredere metabolisk signalering.
Hvordan er Semaglutid og Tirzepatid biokemisk klassificeret?
Semaglutid er biokemisk klassificeret som et langtidsvirkende, lipideret GLP-1-receptoragonistpeptid. Tirzepatid er klassificeret som et langtidsvirkende, lipideret dobbelt inkretinreceptor-agonistpeptid, specifikt en GLP-1R/GIPR co-agonist.

Hielscher Ultrasonics fremstiller højtydende ultralydshomogenisatorer fra Lab til industriel størrelse.