Liposomaalinen semaglutidi voi olla seuraava suuri harppaus GLP-1-lääkkeiden toimittamisessa.
, Kathrin Hielscher, julkaistu Hielscher News -lehdessä
GLP-1-peptideistä, kuten semaglutidista, on tullut yksi viime vuosikymmenen vaikutusvaltaisimmista peptiditerapeuteista, joita käytetään laajasti kliinisesti tyypin 2 diabeteksen ja liikalihavuuden hoidossa. Kliinisestä menestyksestään huolimatta semaglutidin formulointi- ja valmistushaasteet ovat kuitenkin edelleen edustavia peptidilääkkeille yleensä: ne ovat rakenteeltaan hauraita, niitä on vaikea suojata hajoamiselta ja niitä on tunnetusti vaikea toimittaa ei-invasiivisia reittejä käyttäen. Nämä rajoitukset ovat merkittävä syy siihen, että useimmat GLP-1-reseptoriagonistit perustuvat edelleen injektioihin, vaikka oraalisen tai potilasystävällisen annostelun kysyntä kasvaa jatkuvasti.
Nykyisten suun kautta otettavien GLP-1-valmisteiden rajat
Suun kautta otettavien GLP-1-peptidien kehittäminen osoitti, että suun kautta annostelu on teknisesti mahdollista, mutta se paljasti myös nykyisten strategioiden keskeiset rajoitukset. Jopa hyväksytyssä valmisteessa suun kautta otettavan semaglutidin biologinen hyötyosuus on hyvin alhainen, tyypillisesti alle 1 %, mikä edellyttää suurempaa annostelua ja lisää kustannuksia, vaihtelevuutta ja formulaation monimutkaisuutta. Nämä rajoitukset ovat lisänneet kiinnostusta kantaja-ainepohjaisiin järjestelmiin, jotka voivat suojata peptidilääkkeitä ja mahdollisesti parantaa imeytymistä turvautumatta yksinomaan kemiallisiin permeaation tehostajiin.
Liposomit teknisesti kehittyneenä jakelualustana
 Tutkittavista jakelujärjestelmistä liposomaalinen kapselointi erottuu edukseen teknisen kypsyytensä ja farmaseuttisen merkityksensä vuoksi. Liposomit koostuvat fosfolipidikaksoiskerroksista, jotka muistuttavat läheisesti biologisia kalvoja, ja niitä on pitkään käytetty kliinisesti onkologiassa ja tartuntataudeissa. Niiden merkitys peptiditerapeuttisten aineiden kannalta perustuu niiden kykyyn suojata fyysisesti herkkiä vaikuttavia aineita ja samalla niiden kokoa, koostumusta ja pintaominaisuuksia voidaan säätää. Liposomien suorituskyky riippuu kuitenkin voimakkaasti kokojakaumasta, kaksoiskerroksen rakenteesta, lastausstrategiasta ja valmistuksen toistettavuudesta. – tekijät, jotka määräytyvät ensisijaisesti prosessitekniikan eikä niinkään pelkän koostumuksen perusteella.
Tutkittavista jakelujärjestelmistä liposomaalinen kapselointi erottuu edukseen teknisen kypsyytensä ja farmaseuttisen merkityksensä vuoksi. Liposomit koostuvat fosfolipidikaksoiskerroksista, jotka muistuttavat läheisesti biologisia kalvoja, ja niitä on pitkään käytetty kliinisesti onkologiassa ja tartuntataudeissa. Niiden merkitys peptiditerapeuttisten aineiden kannalta perustuu niiden kykyyn suojata fyysisesti herkkiä vaikuttavia aineita ja samalla niiden kokoa, koostumusta ja pintaominaisuuksia voidaan säätää. Liposomien suorituskyky riippuu kuitenkin voimakkaasti kokojakaumasta, kaksoiskerroksen rakenteesta, lastausstrategiasta ja valmistuksen toistettavuudesta. – tekijät, jotka määräytyvät ensisijaisesti prosessitekniikan eikä niinkään pelkän koostumuksen perusteella.
Miksi ultraäänikäsittely on keskeistä liposomien valmistuksessa?
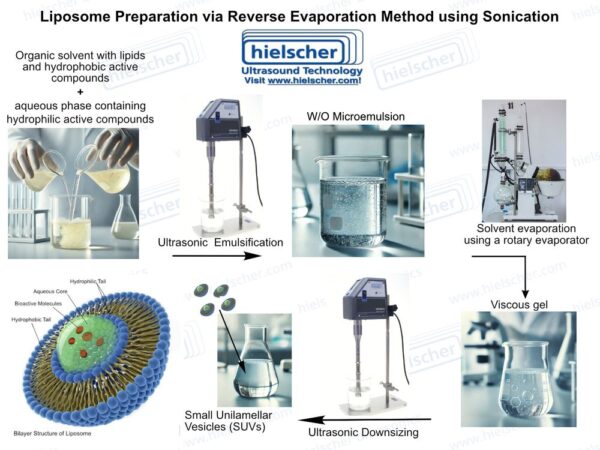
Ultraäänikäsittely ratkaisee useita liposomien valmistukseen liittyviä keskeisiä haasteita. Korkean intensiteetin ultraääni tuottaa akustista kavitaatiota nesteissä, tuottaa paikallisia leikkausvoimia ja mikrosekoitusvaikutuksia, jotka voivat hajottaa lipidien aggregaatteja ja muuntaa multilamellarisia rakenteita pienemmiksi, yhtenäisemmiksi vesikkeleiksi. Liposomien valmistuksessa ultraääntä voidaan käyttää vesikkelien muodostuksen aikana tai jälkikäsittelyvaiheena hiukkaskoon ja dispersion laadun vakioimiseksi. Tämä kaksoisrooli tekee ultraäänestä erityisen arvokkaan liposomijärjestelmien kriittisten laatuominaisuuksien valvonnassa.
Semaglutidin rakenteellinen yhteensopivuus lipidikaksoiskerrosten kanssa
GLP-1-peptidit, kuten semaglutidi tai tirzepatidi, soveltuvat erityisen hyvin lipidipohjaisiin kantajiin, koska ne eivät ole yksinkertaisia lineaarisia peptidejä. Molekyyli sisältää kemiallisesti muunnetun lipidihännän, joka edistää vuorovaikutusta lipidikalvojen kanssa. Vesikkelijärjestelmillä tehdyt kokeelliset tutkimukset ovat osoittaneet, että semaglutidi ja sen sukuiset peptidit voivat assosioitua vesikkelikalvoihin tämän lipidihännän avulla. Vaikka nämä havainnot saatiin käyttämällä maidosta peräisin olevia solunulkoisia vesikkeleitä eikä synteettisiä liposomeja, taustalla oleva mekanismi on suoraan siirrettävissä. Lipidoituneilla peptideillä on luontainen affiniteetti fosfolipidikaksoiskalvoihin, mikä voi parantaa lataustehokkuutta ja formulaation vakautta ilman monimutkaista kemiallista konjugointia.
Prosessiolosuhteet määrittävät kapseloinnin tehokkuuden
Viimeaikaisista vesikkelipohjaisista tutkimuksista on saatu ratkaiseva oivallus, että kapseloinnin tehokkuus riippuu suuresti lastaus- ja käsittelymenetelmästä. Tällä on merkittäviä vaikutuksia lääkekehitykseen: peptidiliposomivalmisteen onnistuminen tai epäonnistuminen ei useinkaan riipu niinkään lipidin valinnasta vaan pikemminkin siitä, miten vesikkelit valmistetaan ja käsitellään. Ultraäänikäsittely tarjoaa hallittavissa olevan ja toistettavissa olevan keinon vaikuttaa näihin parametreihin, mikä tekee siitä erityisen houkuttelevan systemaattisessa formulaatiokehityksessä.
Skaalautuvuus ultraäänikäsittelyn keskeisenä etuna
Valmistuksen kannalta yksi ultraäänen merkittävimmistä eduista on sen skaalautuvuus. Toisin kuin monet nanohiukkasten tuotantotekniikat, jotka perustuvat geometriakohtaisiin eräkohtaisiin olosuhteisiin, ultraäänikäsittelyä voidaan skaalata ohjaamalla energian syöttöä tilavuusyksikköä kohti. Tämän ansiosta laboratoriomittakaavassa kehitetyt prosessit voidaan siirtää pilotti- ja teollisuusjärjestelmiin hyvin vertailukelpoisina. Lääkevalmistajille tämä ominaisuus tukee toistettavuutta, validointia ja tehokasta teknologian siirtoa eri kehitysvaiheissa.
Jatkuvan virtauksen sonikointi teollisessa tuotannossa
Teollisesti merkittävin ultraääni-liposomien käsittelyn toteutus on jatkuva virtaus. Läpivirtaussonikaatiokennoissa liposomidispersiot kulkevat määritellyn reaktoritilavuuden läpi, kun ultraääntä käytetään kontrolloidussa paineessa, amplitudissa ja lämpötilassa. Tämä konfiguraatio mahdollistaa oleskeluaikojen ja energia-altistuksen tarkan hallinnan. Peptidipitoisten liposomien kohdalla, joissa lämpöherkkyys ja rakenteellinen eheys ovat kriittisiä, tällainen valvonta on olennaisen tärkeää tuotteen laadun säilyttämiseksi mittakaavassa.
Merkitys seuraavan sukupolven GLP-1- ja peptiditerapioiden kannalta
GLP-1-hoitojen kehittyessä kohti kaksois- ja moniagonistisia peptidejä formulaatioiden monimutkaisuuden odotetaan lisääntyvän. Samaan aikaan potilaiden kysyntä suun kautta otettavien tai vähemmän invasiivisten antoreittien suhteen kasvaa edelleen. Skaalautuvista kantaja-ainepohjaisista jakelualustoista tulee näin ollen strategisesti tärkeitä paitsi farmakokinetiikan parantamiseksi myös sen varmistamiseksi, että uusia peptidilääkkeitä voidaan valmistaa luotettavasti kaupallisessa mittakaavassa.
Suun kautta annettavien peptidien perimmäisen esteen poistaminen
Ruoansulatuskanava on luonnostaan vihamielinen peptideille, ja alhainen oraalinen hyötyosuus on edelleen perustavanlaatuinen este jopa kehittyneille formulaatioille. Liposomaalinen kapselointi ei poista tätä haastetta, mutta se tarjoaa rationaalisen teknisen lähestymistavan, jolla voidaan vähentää hajoamista ja hallita peptidien vuorovaikutusta suoliston ympäristön kanssa. Yhdistettynä skaalautuviin käsittelytekniikoihin, kuten ultraäänitekniikkaan, liposomipohjaiset jakelujärjestelmät ovat lähempänä teollista toteutettavuutta sen sijaan, että ne jäisivät laboratoriokokeisiin.
Laboratoriokehityksestä teolliseen käyttöönottoon
 Käytännön kehitystyönkuluissa Hielscher Ultrasonics -järjestelmiä käytetään usein referenssialustoina liposomien ultraäänikäsittelyssä. Laboratorio- ja formulaatiokehityksen mittakaavassa kompaktit ultraäänianturit, kuten UP200Ht ja UP400St, mahdollistavat hallitun pienerien käsittelyn ja menetelmän optimoinnin. Teollista valmistusta varten läpivirtausreaktoreilla varustetut sonikaattorit tukevat jatkuvaa toimintaa, suurta tehotiheyttä ja lineaarista skaalautumista. Nämä ominaisuudet vastaavat farmaseuttisten tuotantoympäristöjen vaatimuksia, mukaan lukien prosessin valvonta ja toistettavuus.
Käytännön kehitystyönkuluissa Hielscher Ultrasonics -järjestelmiä käytetään usein referenssialustoina liposomien ultraäänikäsittelyssä. Laboratorio- ja formulaatiokehityksen mittakaavassa kompaktit ultraäänianturit, kuten UP200Ht ja UP400St, mahdollistavat hallitun pienerien käsittelyn ja menetelmän optimoinnin. Teollista valmistusta varten läpivirtausreaktoreilla varustetut sonikaattorit tukevat jatkuvaa toimintaa, suurta tehotiheyttä ja lineaarista skaalautumista. Nämä ominaisuudet vastaavat farmaseuttisten tuotantoympäristöjen vaatimuksia, mukaan lukien prosessin valvonta ja toistettavuus.
Semaglutidin lisäksi: Semagutagid: Alustan näkökulma
Vaikka semaglutidi on erittäin merkityksellinen malliyhdiste, ultraääniliposomien kapseloinnin vaikutukset ulottuvat yksittäistä vaikuttavaa ainetta laajemmalle. Sama prosessilogiikka pätee muihin lipidoituihin peptideihin, peptidikonjugaatteihin ja uusiin biologisiin lääkkeisiin. Kun peptiditerapiat laajenevat aineenvaihduntasairauksien, onkologian ja immunologian alalla, skaalautuvista kapselointiteknologioista tulee todennäköisesti ratkaisevia tekijöitä määriteltäessä, mitkä toimitusstrategiat voivat edetä konseptista kaupalliseen todellisuuteen.
Siirtyminen kohti prosessiteknisesti suunniteltua peptidien toimittamista
Ultraäänikapseloitu liposomaalinen semaglutidi on osoitus laajemmasta muutoksesta lääkekehityksessä: ensisijaisesti biologisten perusteiden ohjaamista formulaatiokonsepteista siirrytään prosessitekniikkaan ja valmistettavuuteen perustuviin toimitusjärjestelmiin. Alalla, jolla monet suun kautta otettavat peptiditeknologiat epäonnistuvat skaalausvaiheessa, ultraäänellä tapahtuva liposomien käsittely tarjoaa verrattain suoran ja teknisesti vankan väylän laboratoriokehityksestä teolliseen tuotantoon.
Kirjallisuus / Viitteet
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
Usein Kysytyt Kysymykset
Mitä ovat GLP-1-peptidit?
GLP-1-peptidit ovat inkretiinimimeettisiä peptidilääkkeitä, jotka aktivoivat glukagonin kaltaista peptidi-1-reseptoria (GLP-1R), joka on keskeinen metabolinen reseptori, joka osallistuu glukoosiriippuvaiseen insuliinin eritykseen, glukagonin vapautumisen estoon, viivästyneeseen mahalaukun tyhjenemiseen ja ruokahalun säätelyyn. Kliinisesti käytetyt GLP-1-peptidit (kuten semaglutidi) on muunnettu kemiallisesti entsymaattisen hajoamisen estämiseksi ja kiertoaikojen pidentämiseksi natiiviin GLP-1:een verrattuna.
Mitä eroa on semaglutidin ja tirzepatidin välillä?
Semaglutidi on yksiagonistinen peptidi, joka aktivoi selektiivisesti glukagonin kaltaisen peptidi-1-reseptorin (GLP-1R), kun taas tirzepatidi on kaksoisagonisti, joka aktivoi sekä GLP-1-reseptorin että glukoosiriippuvaisen insuliinotrooppisen polypeptidireseptorin (GIPR). Biokemiallisesti tirzepatidi on suurempi ja monimutkaisempi peptidi, jonka sekvenssielementit ja reseptoria sitovat domeenit on optimoitu kahden inkretiinireseptorin aktivoimiseksi, kun taas semaglutidi on suunniteltu erityisesti korkean affiniteetin GLP-1R-aktivaatiota varten. Molemmat peptidit on kemiallisesti muunnettu lipidiosuuksilla plasmaproteiiniin sitoutumisen lisäämiseksi ja systeemisen puoliintumisajan pidentämiseksi, mutta tirzepatidin kahden reseptorin aktiivisuus johtaa laajempaan metaboliseen signalointiin.
Miten semaglutidi ja tirzepatidi luokitellaan biokemiallisesti?
Semaglutidi luokitellaan biokemiallisesti pitkävaikutteiseksi, lipidoituneeksi GLP-1-reseptoriagonistipeptidiksi. Tirzepatidi luokitellaan pitkävaikutteiseksi, lipidoituneeksi kaksoisinkretiinireseptoriagonistipeptidiksi, erityisesti GLP-1R/GIPR-koagonistiksi.

Hielscher Ultrasonics valmistaa korkean suorituskyvyn ultraäänihomogenisaattoreita laboratorio jotta Teollisuuden koko.