Ultradźwiękowe kapsułkowanie liposomów peptydów GLP-1: Skalowalna technologia doustnego dostarczania peptydów
Semaglutyd i inne peptydy GLP-1 zmieniają sposób leczenia cukrzycy i otyłości, ale większość leków peptydowych nadal wymaga zastrzyków, ponieważ doustne podawanie pozostaje niezwykle trudne. Nawet zatwierdzony doustny semaglutyd wykazuje biodostępność poniżej 1%, co zwiększa wymagania dotyczące dawki i koszty. Zamknięcie peptydów GLP-1 w liposomach może przezwyciężyć te ograniczenia. Dowiedz się, w jaki sposób ultradźwiękowe przygotowanie liposomów ułatwia liposomy obciążone peptydem GLP-1 w aptekach złożonych i produkcji farmaceutycznej.
Liposomalne peptydy GLP-1
Agoniści receptora GLP-1, tacy jak semaglutyd i peptydy inkretynowe nowej generacji, takie jak tirzepatyd, zmieniły sposób leczenia cukrzycy typu 2 i otyłości. Jednak z punktu widzenia formulacji i produkcji, te API nadal mają klasyczne ograniczenia leków peptydowych: są kruche, łatwo ulegają degradacji i trudno je dostarczyć przez przewód pokarmowy.
Dlatego też większość peptydów GLP-1 pozostaje w formie iniekcji, mimo że podawanie doustne znacznie zmniejszyłoby bariery dla pacjentów. Podawanie doustne ogólnie poprawia wygodę, przestrzeganie zaleceń i chęć wcześniejszego rozpoczęcia terapii – zwłaszcza w chorobach przewlekłych.
Jednak doustne podawanie peptydów pozostaje jednym z najtrudniejszych wyzwań w naukach farmaceutycznych. Nawet zatwierdzone doustne produkty semaglutydu wykazują bardzo niską biodostępność, wymagając wysokich dawek i starannych strategii formułowania.
Jednym z najbardziej obiecujących podejść technicznych do przezwyciężenia tych ograniczeń jest enkapsulacja liposomalna w połączeniu z przetwarzaniem ultradźwiękowym o wysokiej intensywności. Liposomy chronią peptydowe API, poprawiają stabilność dyspersji i mogą być zaprojektowane dla zakresów wielkości w skali nano, które są istotne dla penetracji śluzu i interakcji jelitowych. Sonikacja zapewnia skalowalną i powtarzalną metodę produkcji tych liposomów w ilościach istotnych dla przemysłu.
Dlaczego liposomy są silną platformą dla peptydów GLP-1?
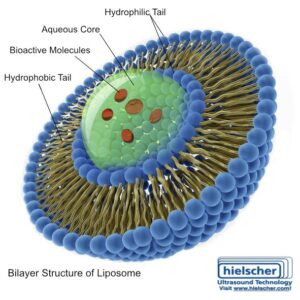 Liposomy to pęcherzyki utworzone przez dwuwarstwy fosfolipidowe, podobne w składzie do błon biologicznych. To sprawia, że są one z natury biokompatybilne i dobrze nadają się do rozwoju farmaceutycznego. W przypadku leków peptydowych liposomy są atrakcyjne, ponieważ mogą fizycznie chronić substancję czynną (API) i zapewniają architekturę formulacji, którą można dostosować do wydajności dostarczania.
Liposomy to pęcherzyki utworzone przez dwuwarstwy fosfolipidowe, podobne w składzie do błon biologicznych. To sprawia, że są one z natury biokompatybilne i dobrze nadają się do rozwoju farmaceutycznego. W przypadku leków peptydowych liposomy są atrakcyjne, ponieważ mogą fizycznie chronić substancję czynną (API) i zapewniają architekturę formulacji, którą można dostosować do wydajności dostarczania.
W kontekście peptydów GLP-1 kluczowym wyzwaniem jest nie tylko ochrona peptydu przed kwasami i enzymami, ale także umożliwienie znaczącego wchłaniania przez barierę jelitową. Jest to wielowarstwowy problem obejmujący pH, degradację enzymatyczną, transport śluzu, przepuszczalność nabłonka i mechanizmy transportu.
Literatura naukowa w coraz większym stopniu wspiera koncepcję, że nośniki oparte na pęcherzykach mogą poprawić stabilność peptydów i interakcję z układami jelitowymi.
Dlaczego semaglutyd jest szczególnie interesujący do kapsułkowania liposomalnego?
Semaglutyd to nie tylko peptyd – Jest to peptyd z wbudowaną modyfikacją ogona lipidowego. Jest to kluczowy powód, dla którego zachowuje się inaczej niż wiele innych peptydowych API w układach lipidowych.
Peptydy GLP-1, takie jak semaglutyd i tirzepatyd, ładują się do pęcherzyków poprzez wprowadzenie ogona lipidowego do błony pęcherzykowej.
Z punktu widzenia inżynierii jest to ważne, ponieważ sugeruje, że semaglutyd jest strukturalnie kompatybilny z dwuwarstwami lipidowymi, co oznacza, że może być możliwe osiągnięcie stabilnego połączenia i znaczącego obciążenia bez nadmiernej modyfikacji chemicznej.
Ta sama logika ma zastosowanie do innych lipidowanych peptydowych API i koniugatów peptyd-lek.
Rzeczywistość produkcyjna: Liposomy muszą być odtwarzalne i skalowalne
Enkapsulacja liposomów nie jest trudna w laboratorium. Prawdziwa trudność zaczyna się, gdy preparat musi być wytwarzany w powtarzalny sposób na dużą skalę.
Przemysłowa produkcja liposomów musi być kontrolowana:
- rozkład wielkości liposomów
- polidyspersyjność
- wydajność hermetyzacji
- stabilność dyspersji
- powtarzalność między partiami
- Kompatybilność ze sterylnym przetwarzaniem
- walidacja i dokumentacja procesu
Wiele popularnych metod liposomowych (worteksowanie, proste nawilżanie, ręczne wyciskanie) może dawać dobre wyniki na stanowisku badawczym - ale zawodzą, gdy są przenoszone do pilotażowych lub produkcyjnych wolumenów.
W tym miejscu przetwarzanie ultradźwiękowe staje się kluczową technologią wspomagającą.
Ultradźwiękowa enkapsulacja liposomów: Podstawowa zasada
Ultradźwięki o wysokiej intensywności wprowadzają energię mechaniczną do cieczy poprzez kawitację akustyczną. Kawitacja polega na tworzeniu się i zapadaniu mikroskopijnych pęcherzyków, wytwarzając zlokalizowane siły ścinające i efekty mikromieszania.
W dyspersjach lipidowych siły te:
- tworzenie mikroemulsji w celu zainicjowania formowania liposomów
- rozbijają duże agregaty lipidowe
- redukują struktury wielokomórkowe
- generują mniejsze, bardziej jednolite pęcherzyki
- poprawić homogenizację
- zwiększenie powtarzalności końcowej dyspersji
Przetwarzanie ultradźwiękowe jest zatem szeroko stosowane w produkcji nanomateriałów, emulgowaniu i dyspersji - i jest wysoce odpowiednie do nano-rozmiaru liposomów.
W przypadku liposomów peptydowych GLP-1, ultradźwięki mogą być stosowane albo do tworzenia liposomów bezpośrednio podczas hydratacji i dyspersji, albo jako etap przetwarzania końcowego w celu udoskonalenia wielkości pęcherzyków i poprawy jednorodności.
Dlaczego ultradźwięki są szczególnie cenne w farmaceutycznej produkcji liposomów?
Najważniejszym powodem, dla którego ultradźwięki są wykorzystywane w przemyśle, jest to, że można je skalować poprzez kontrolowanie mierzalnego parametru procesu: energii na objętość.
Zamiast skalowania przez “Więcej miksowania” lub “dłuższe przetwarzanie,” Systemy ultradźwiękowe umożliwiają skalowanie procesu:
- zwiększenie mocy ultradźwięków
- zwiększenie natężenia przepływu
- utrzymując ten sam pobór energii na ml
- przy użyciu reaktorów o przepływie ciągłym
- numeracja równoległa
Sprawia to, że proces ten może być w dużym stopniu przenoszony z R&D do produkcji.
W praktyce oznacza to, że proces liposomowy opracowany na małym systemie może zostać przeniesiony do większych systemów przy zachowaniu równoważnych warunków procesu, co jest dokładnie tym, czego wymaga produkcja farmaceutyczna.
Wpływ na peptydy GLP-1: W kierunku lepszej biodostępności po podaniu doustnym
Podawanie doustne jest długoterminowym celem dla wielu preparatów peptydów GLP-1. Powód jest prosty: jeśli poprawi się biodostępność po podaniu doustnym, cała terapia stanie się łatwiejsza dla pacjentów.
Przesłany materiał podkreśla obecne ograniczenia: doustne stosowanie semaglutydu jest możliwe, ale biodostępność pozostaje niska (poniżej 1%).
Enkapsulacja liposomowa nie gwarantuje wysokiej biodostępności po podaniu doustnym, ale rozwiązuje jednocześnie kilka krytycznych wąskich gardeł:
- Może fizycznie chronić peptyd przed degradacją.
- Może ona tworzyć nanonośniki o właściwościach dostosowanych do penetracji śluzu.
- Może być sfunkcjonalizowany ligandami powierzchniowymi dla aktywnych mechanizmów transportu.
- Może to poprawić spójność i powtarzalność dostarczanej formy API.
W szczególności w przypadku semaglutydu, asocjacja błonowa poprzez ogon lipidowy zapewnia dodatkowy mechanizm, który może stabilizować peptyd w układach lipidowych.
Przetwarzanie ultradźwiękowe umożliwia ciągłą, przemysłową produkcję liposomów
W produkcji przemysłowej często preferowane jest przetwarzanie ciągłe, ponieważ poprawia ono wydajność:
- Przepustowość
- odtwarzalność
- kontrola procesu
- integracja ze sterylnymi procesami produkcyjnymi
Idealnie nadają się do tego ultradźwiękowe systemy przepływowe. Dyspersja liposomów jest pompowana przez ciśnieniową komorę przepływową, w której ultradźwięki są stosowane w kontrolowanych warunkach. Temperatura, ciśnienie i czas przebywania mogą być kontrolowane, co jest niezbędne w przypadku preparatów peptydowych.
Umożliwia to skalowalne procesy nano-rozmiaru i enkapsulacji, które są znacznie bliższe wymaganiom GMP niż wiele metod laboratoryjnych.
Hielscher Ultrasonics: Systemy laboratoryjno-przemysłowe do kapsułkowania liposomów

Hielscher Ultrasonics dostarcza systemy ultradźwiękowe, które pasują do rzeczywistej ścieżki rozwoju liposomalnych preparatów peptydowych.
W skali laboratoryjnej UP400St jest szeroko stosowany do badań przesiewowych formulacji, opracowywania procesów i przygotowywania liposomów na skalę mieszaną.
W skali produkcyjnej, UIP2000hdT i UIP4000hdT są przeznaczone do przemysłowych cykli pracy i mogą być zintegrowane z przepływowymi komórkami sonikacyjnymi do ciągłego przetwarzania.
Ta kombinacja jest szczególnie istotna dla produkcji liposomów farmaceutycznych, ponieważ wspiera:
- powtarzalność procesu
- liniowa skalowalność
- produkcja w trybie ciągłym
- Przetwarzanie ultradźwiękowe o dużej mocy w kontrolowanych warunkach

Sonicator UIP1000hdT ze szklaną komorą przepływową do produkcji liposomów.
W skrócie – Dlaczego ultradźwiękowa formulacja liposomowa peptydów GLP-1
Ultradźwiękowa enkapsulacja liposomów jest jednym z najbardziej dojrzałych technicznie i skalowalnych przemysłowo podejść do produkcji liposomów obciążonych peptydami. W przypadku peptydów GLP-1, takich jak semaglutyd i tirzepatyd, podejście to jest szczególnie istotne, ponieważ te API są strukturalnie kompatybilne z błonami lipidowymi i mogą korzystać ze strategii ochrony i dostarczania opartych na pęcherzykach.
Co najważniejsze, ultradźwięki nie są jedynie metodą laboratoryjną – Jest to skalowalna technologia procesowa. Kontrolując pobór energii na objętość i wykorzystując przepływowe komórki sonikacyjne, przetwarzanie ultradźwiękowe można przenieść z rozwoju w skali laboratoryjnej do pilotażowej i pełnej produkcji przemysłowej.
Ponieważ przemysł farmaceutyczny nadal zmierza w kierunku terapii peptydowych – a wraz z rosnącym zapotrzebowaniem na przyjazne dla pacjentów trasy dostaw – Ultradźwiękowa produkcja liposomów będzie odgrywać coraz większą rolę w tworzeniu preparatów GLP-1 nowej generacji.
Poniższa tabela przedstawia przybliżoną wydajność przetwarzania naszych ultradźwiękowców:
| Wielkość partii | natężenie przepływu | Polecane urządzenia |
|---|---|---|
| 0.5-1,5 mL | b.d. | VialTweeter |
| 1 do 500mL | 10-200mL/min | UP100H |
| 10 do 2000mL | 20-400mL/min | UP200Ht, UP400St |
| 0.1 do 20L | 0.2 do 4L/min | UIP2000hdT |
| 10-100L | 2 do 10L/min | UIP4000hdT |
| 15 do 150 l | 3 do 15 l/min | UIP6000hdT |
| b.d. | 10-100L/min | UIP16000hdT |
| b.d. | większe | klaster UIP16000hdT |
Projektowanie, produkcja i doradztwo – Jakość Made in Germany
Ultradźwięki Hielscher są dobrze znane z najwyższej jakości i standardów projektowych. Solidność i łatwa obsługa pozwalają na płynną integrację naszych ultradźwiękowców z obiektami przemysłowymi. Trudne warunki i wymagające środowiska są łatwo obsługiwane przez ultradźwięki Hielscher.
Hielscher Ultrasonics jest firmą posiadającą certyfikat ISO i kładzie szczególny nacisk na wysokowydajne ultradźwięki z najnowocześniejszą technologią i łatwością obsługi. Oczywiście ultradźwięki Hielscher są zgodne z CE i spełniają wymagania UL, CSA i RoHs.
Literatura / Referencje
- Martyna Truszkowska; Ahmad Saleh; Melanie Lena Eber; Gergely Kali; Andreas Bernkop-Schnürch (2025): Addressing the polycation dilemma in drug delivery: charge-converting liposomes. Journal of Materials Chemistry B 2025, 13, 9100-9111.
- Pop, R.; Nistor, M.; Socaciu, C.; Cenariu, M.; Tăbăran, F.; Rugină, D.; Pintea, A.; Socaciu, M.A. (2025): Distinct In Vitro Effects of Liposomal and Nanostructured Lipid Nanoformulations with Entrapped Acidic and Neutral Doxorubicin on B16-F10 Melanoma and Walker 256 Carcinoma Cells. Pharmaceutics 2025, 17, 904.
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
często zadawane pytania
Jaką rolę odgrywa emulgowanie ultradźwiękowe w tworzeniu liposomów?
Ultradźwiękowa emulsyfikacja fazy wodnej i lipidów zapewnia energię mechaniczną wymaganą do drobnego rozproszenia lipidów w wodzie i napędzania ich samoorganizacji w zamknięte struktury dwuwarstwowe. Kawitacja akustyczna generowana przez ultradźwięki tworzy intensywne mikromieszanie i siły ścinające, które rozdrabniają fazy lipidowe, równomiernie nawilżają cząsteczki lipidów i przekształcają rozproszone fragmenty lipidów w pęcherzyki liposomalne. Promuje to szybkie tworzenie pęcherzyków, redukuje struktury wielokomórkowe i daje mniejsze, bardziej jednolite liposomy o lepszej powtarzalności i stabilności.
Co powinienem wiedzieć o formułowaniu GLP-1?
Peptydy GLP-1 są wysoce skutecznymi lekami, ale większość z nich można wstrzykiwać ze względu na degradację w przewodzie pokarmowym i bariery wchłaniania.
Istnieje doustny semaglutyd, ale zgłaszana biodostępność pozostaje poniżej 1%.
Semaglutyd i tirzepatyd mogą być ładowane do systemów pęcherzykowych, a skuteczność ładowania zależy w dużym stopniu od metody przetwarzania.
Semaglutyd może wiązać się z błonami lipidowymi poprzez swój ogon lipidowy, wspierając kompatybilność pęcherzyków/liposomów.
Kawitacja ultradźwiękowa umożliwia powtarzalną nano-rozmianę liposomów i homogenizację dyspersji.
Ultradźwięki skalują się liniowo dzięki kontroli energii na objętość i ciągłemu przetwarzaniu przepływu.
Systemy Hielscher obsługują pełny przepływ pracy:
- UP400St (skala laboratoryjna i złożona)
- UIP2000hdT / UIP4000hdT + komórki przepływowe (przemysłowa produkcja farmaceutyczna)
Czym są peptydy GLP-1?
Peptydy GLP-1 są opartymi na peptydach agonistami receptorów inkretynowych, które naśladują lub zwiększają aktywność biologiczną glukagonopodobnego peptydu-1 (GLP-1), hormonu jelitowego zaangażowanego w zależne od glukozy wydzielanie insuliny, hamowanie uwalniania glukagonu oraz regulację opróżniania żołądka i apetytu. Stosowane klinicznie leki GLP-1 (np. semaglutyd) są modyfikowane chemicznie, aby były odporne na degradację enzymatyczną i osiągały długi ogólnoustrojowy okres półtrwania.
Jak powszechnie podaje się peptydy GLP-1?
Większość peptydów GLP-1 podaje się we wstrzyknięciach podskórnych, ponieważ peptydy są niestabilne w przewodzie pokarmowym i mają bardzo niską przepuszczalność jelitową. Podawanie doustne semaglutydu zostało osiągnięte przy użyciu specjalistycznych strategii formułowania, ale biodostępność po podaniu doustnym pozostaje niska (około 0,4%-1%).
Jakie są zalety doustnego podawania liposomów peptydu GLP-1?
Doustne liposomy peptydu GLP-1 mogą poprawić wygodę pacjenta i przestrzeganie zaleceń poprzez wyeliminowanie zastrzyków, jednocześnie potencjalnie zwiększając skuteczne wchłanianie poprzez ochronę peptydów przed degradacją kwasową i enzymatyczną oraz poprawę transportu przez śluz i bariery nabłonkowe. Lepsza biodostępność doustna może zmniejszyć obciążenie dawką, obniżyć presję kosztową i zmniejszyć bariery dla pacjentów w rozpoczęciu i utrzymaniu długoterminowej terapii peptydowej.

Hielscher Ultrasonics produkuje wysokowydajne homogenizatory ultradźwiękowe od laboratorium do rozmiar przemysłowy.



