Liposomaalne semaglutiid võib olla järgmine suur hüpe GLP-1 ravimi manustamisel
, Kathrin Hielscher, avaldatud Hielscheri uudistes
GLP-1-peptiidid, nagu semaglutiid, on muutunud viimasel kümnendil üheks kõige mõjukamaks peptiidravimiks, mida kasutatakse laialdaselt kliiniliselt 2. tüüpi diabeedi ja rasvumise puhul. Kuid vaatamata kliinilisele edule on semaglutiidi formuleerimis- ja tootmisprobleemid endiselt iseloomulikud peptiidravimitele üldiselt: need on struktuuriliselt haprad, neid on raske kaitsta lagunemise eest ja neid on teatavasti raske manustada mitteinvasiivsetel viisidel. Need piirangud on peamine põhjus, miks enamik GLP-1 retseptori agoniste on ikka veel süstides, isegi kui nõudlus suukaudse või patsiendisõbraliku manustamise järele kasvab.
Praeguste suukaudsete GLP-1 preparaatide piirid
Suukaudsete GLP-1 peptiidide väljatöötamine näitas, et suukaudne manustamine on tehniliselt võimalik, kuid see tõi esile ka olemasolevate strateegiate peamised piirangud. Isegi heakskiidetud toote puhul on suukaudse semaglutiidi biosaadavus väga madal, tavaliselt alla 1%, mis nõuab suuremat annustamist ning suurendab kulusid, varieeruvust ja koostise keerukust. Need piirangud on suurendanud huvi kandjal põhinevate süsteemide vastu, mis suudavad kaitsta peptiidravimeid ja potentsiaalselt parandada imendumist, ilma et nad tugineksid ainult keemilistele permeatsioonitugevdajatele.
Liposoomid kui tehniliselt küpsed manustamisplatvormid
 Uuritavates manustamissüsteemides paistab liposomaalne kapseldamine silma oma tehnilise küpsuse ja farmatseutilise asjakohasuse poolest. Liposoomid koosnevad fosfolipiidide kaksikkihist, mis sarnanevad lähedalt bioloogilistele membraanidele ja mida on pikka aega kliiniliselt kasutatud onkoloogias ja nakkushaigustes. Nende tähtsus peptiidravimite jaoks seisneb nende võimes kaitsta füüsiliselt tundlikke toimeaineid, pakkudes samal ajal reguleeritavat suurust, koostist ja pinnaomadusi. Liposoomide toimivus sõltub siiski tugevalt suuruse jaotusest, kahekihilise kihi struktuurist, laadimisstrateegiast ja tootmise reprodutseeritavusest. – tegurid, mida reguleerib peamiselt protsessitehnoloogia, mitte ainult koostis.
Uuritavates manustamissüsteemides paistab liposomaalne kapseldamine silma oma tehnilise küpsuse ja farmatseutilise asjakohasuse poolest. Liposoomid koosnevad fosfolipiidide kaksikkihist, mis sarnanevad lähedalt bioloogilistele membraanidele ja mida on pikka aega kliiniliselt kasutatud onkoloogias ja nakkushaigustes. Nende tähtsus peptiidravimite jaoks seisneb nende võimes kaitsta füüsiliselt tundlikke toimeaineid, pakkudes samal ajal reguleeritavat suurust, koostist ja pinnaomadusi. Liposoomide toimivus sõltub siiski tugevalt suuruse jaotusest, kahekihilise kihi struktuurist, laadimisstrateegiast ja tootmise reprodutseeritavusest. – tegurid, mida reguleerib peamiselt protsessitehnoloogia, mitte ainult koostis.
Miks ultrahelitöötlus on liposoomide valmistamisel keskse tähtsusega
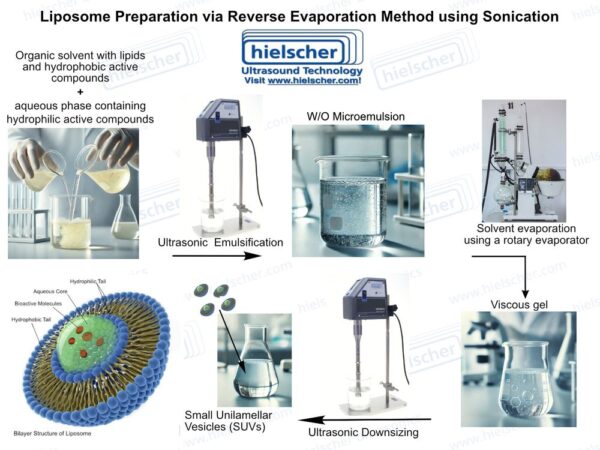
Ultrahelitöötlus lahendab mitmeid peamisi probleeme, mis on seotud liposoomide tootmisega. Kõrge intensiivsusega ultraheli tekitab vedelikes akustilist kavitatsiooni, tekitades lokaalseid nihkejõude ja mikrosegamise efekte, mis võivad lagundada lipiidagregaate ja teisendada multilamellaarseid struktuure väiksemateks, ühtlasemateks vesikliteks. Liposoomide tootmisel võib ultraheli kasutada vesiklite moodustamise ajal või järeltöötlemisetapina, et standardida osakeste suurust ja dispersiooni kvaliteeti. See kahesugune roll muudab ultraheli eriti väärtuslikuks liposoomsete süsteemide kriitiliste kvaliteediomaduste kontrollimisel.
Semaglutiidi struktuuriline kokkusobivus lipiidkihiga
GLP-1 peptiidid, nagu semaglutiid või tirzepatiid, sobivad eriti hästi lipiidipõhiste kandjate jaoks, sest see ei ole lihtne lineaarne peptiid. Molekul sisaldab keemiliselt modifitseeritud lipiidsaba, mis soodustab koostoimet lipiidmembraanidega. Katselised uuringud vesiklisüsteemidega on näidanud, et semaglutiid ja sellega seotud peptiidid võivad assotsieeruda vesikliimembraanidega selle lipiidsaba sisestamise kaudu. Kuigi need tulemused saadi piimast saadud ekstratsellulaarsete vesiklite, mitte sünteetiliste liposoomide abil, on aluseks olev mehhanism otseselt ülekantav. Lipidiseeritud peptiididel on loomupärane afiinsus fosfolipiidkihide suhtes, mis võib parandada laadimise tõhusust ja preparaadi stabiilsust, ilma et oleks vaja keerulist keemilist konjugeerimist.
Protsessi tingimused määravad kapseldamise tõhususe
Hiljutistest vesikliidel põhinevatest uuringutest saadud kriitiline arusaam on, et kapseldumise tõhusus sõltub suuresti laadimis- ja töötlemismeetodist. Sellel on oluline mõju farmaatsia arendamisele: peptiidiliposoomi preparaadi edu või ebaõnnestumine sõltub sageli vähem lipiidi valikust ja rohkem sellest, kuidas vesikleid toodetakse ja töödeldakse. Ultrahelitöötlus pakub kontrollitavat ja korratavat vahendit nende parameetrite mõjutamiseks, mis muudab selle eriti atraktiivseks süstemaatiliseks preparaatide arendamiseks.
Skaleeritavus kui ultrahelitöötluse peamine eelis
Tootmise seisukohalt on ultraheli üks olulisemaid eeliseid selle skaleeritavus. Erinevalt paljudest nanoosakeste tootmismeetoditest, mis sõltuvad geomeetriaspetsiifilistest partiitingimustest, saab ultrahelitöötlust skaleerida, kontrollides energiakulu ühiku mahu kohta. See võimaldab laboratoorsel skaalal välja töötatud protsesse üle viia piloot- ja tööstussüsteemidesse suure võrreldavusega. Ravimitootjate jaoks toetab see omadus reprodutseeritavust, valideerimist ja tõhusat tehnoloogiasiiret eri arendusetappides.
Pidev voolu sonikatsioon tööstuslikuks tootmiseks
Tööstuslikult kõige asjakohasem ultraheli liposoomide töötlemise rakendus on pidev vooluoperatsioon. Läbivoolus sonikatsioonikambris läbivad liposoomidispersioonid kindlaksmääratud reaktori mahtu, samal ajal kui ultraheli rakendatakse kontrollitud rõhu, amplituudi ja temperatuuri all. See konfiguratsioon võimaldab täpset kontrolli viibimisaja ja energia kokkupuute üle. Peptiididega koormatud liposoomide puhul, kus termiline tundlikkus ja struktuuriline terviklikkus on kriitilised, on selline kontroll oluline toote kvaliteedi säilitamiseks mastaabis.
Olulisus järgmise põlvkonna GLP-1 ja peptiidterapeutikumide jaoks
Kuna GLP-1 ravimeetodid arenevad kahe- ja mitmeagonistiliste peptiidide suunas, suureneb eeldatavasti ka koostise keerukus. Samal ajal kasvab patsientide nõudlus suukaudsete või vähem invasiivsete manustamisviiside järele. Seepärast muutuvad skaleeritavad kandjal põhinevad manustamisplatvormid strateegiliselt oluliseks mitte ainult farmakokineetika parandamiseks, vaid ka selleks, et tagada uute peptiidravimite usaldusväärne tootmine kaubanduslikus mahus.
Peptiidide suukaudse manustamise põhitõkke kõrvaldamine
Seedetrakt on peptiidide suhtes loomupäraselt vaenulik ja madal suukaudne biosaadavus on põhiline takistus isegi täiustatud preparaatide puhul. Liposomaalne kapseldamine ei kõrvalda seda probleemi, kuid pakub ratsionaalset tehnilist lähenemist, et vähendada lagunemist ja kontrollida peptiidide koostoimet soolestiku keskkonnaga. Kombineerituna skaleeritavate töötlemistehnoloogiatega, nagu ultraheli, liiguvad liposoomipõhised manustamissüsteemid lähemale tööstuslikule teostatavusele, mitte ei jää laboratoorseteks katseteks.
Laboratoorse arenduse ja tööstusliku rakendamise vahel
 Praktilistes arendusprotsessides kasutatakse Hielscher Ultrasonics'i süsteeme sageli võrdlusplatvormidena ultraheli liposoomide töötlemiseks. Laboratooriumis ja preparaatide arendamise skaalal võimaldavad kompaktsed ultrahelisondid, nagu UP200Ht ja UP400St, kontrollitud väikepartii töötlemist ja meetodi optimeerimist. Tööstusliku tootmise jaoks toetavad läbivoolureaktoritega varustatud sonikaatorid pidevat tööd, suurt võimsustihedust ja lineaarset suurendamist. Need omadused on kooskõlas farmaatsiatootmise keskkonnas kehtivate nõuetega, sealhulgas protsessi kontrolli ja reprodutseeritavusega.
Praktilistes arendusprotsessides kasutatakse Hielscher Ultrasonics'i süsteeme sageli võrdlusplatvormidena ultraheli liposoomide töötlemiseks. Laboratooriumis ja preparaatide arendamise skaalal võimaldavad kompaktsed ultrahelisondid, nagu UP200Ht ja UP400St, kontrollitud väikepartii töötlemist ja meetodi optimeerimist. Tööstusliku tootmise jaoks toetavad läbivoolureaktoritega varustatud sonikaatorid pidevat tööd, suurt võimsustihedust ja lineaarset suurendamist. Need omadused on kooskõlas farmaatsiatootmise keskkonnas kehtivate nõuetega, sealhulgas protsessi kontrolli ja reprodutseeritavusega.
Semaglutiidist kaugemale: Platvormi perspektiiv
Kuigi semaglutiid on väga asjakohane mudelühend, ulatub ultraheli liposoomi kapseldamise mõju kaugemale kui üks toimeaine. Sama protsessiloogika kehtib ka teiste lipiididega peptiidide, peptiidkonjugaatide ja uute bioloogiliste ravimite kohta. Kuna peptiidteraapiad laienevad ainevahetushaiguste, onkoloogia ja immunoloogia valdkonnas, saavad skaleeritavad kapseldamistehnoloogiad tõenäoliselt otsustavateks teguriteks, mis määravad, millised manustamisstrateegiad saavad kontseptsioonist edasi liikuda kaubandusliku reaalsuseni.
Üleminek protsessipõhise peptiidide manustamise suunas
Ultraheli kapseldatud liposomaalne semaglutiid illustreerib laiemat muutust farmaatsiaarenduses: peamiselt bioloogilisest loogikast lähtuvatest preparaadi kontseptsioonidest pöördutakse protsessitehnika ja valmistatavuse põhinevate manustamissüsteemide poole. Valdkonnas, kus paljud suukaudsed peptiiditehnoloogiad ebaõnnestuvad mastaapimisel, pakub ultraheli liposoomide töötlemine suhteliselt otsest ja tehniliselt tugevat teed laboratoorse arenduse ja tööstusliku tootmise vahel.
Kirjandus / Viited
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
Korduma kippuvad küsimused
Mis on GLP-1 peptiidid?
GLP-1-peptiidid on inkretiini-mimeetilised peptiidravimid, mis aktiveerivad glükagooni sarnase peptiidi-1 retseptorit (GLP-1R), mis on peamine metaboolne retseptor, mis on seotud glükoosist sõltuva insuliini sekretsiooni, glükagooni vabanemise pärssimisega, mao tühjenemise hilinemisega ja söögiisu reguleerimisega. Kliiniliselt kasutatavad GLP-1-peptiidid (nt semaglutiid) on keemiliselt modifitseeritud, et nad oleksid ensümaatilisele lagunemisele vastupidavad ja saavutaksid pikema ringlemisaja võrreldes natiivse GLP-1-ga.
Mis on erinevus semaglutiidi ja tirzepatidi vahel?
Semaglutiid on ühe agonistiga peptiid, mis aktiveerib selektiivselt glükagooni sarnase peptiidi-1 retseptorit (GLP-1R), samas kui tirzepatiid on topeltagonist, mis aktiveerib nii GLP-1 retseptorit kui ka glükoosist sõltuva insulinotroopse polüpeptiidi retseptorit (GIPR). Biokeemiliselt on tirzepatiid suurem ja keerulisem peptiid, mille järjestuselemendid ja retseptorit siduvad domeenid on optimeeritud kahe inkretiiniretseptori aktiveerimiseks, samas kui semaglutiid on loodud spetsiaalselt kõrge afiinsusega GLP-1R-i aktiveerimiseks. Mõlemad peptiidid on keemiliselt modifitseeritud lipiidühenditega, et suurendada plasmavalkudega seondumist ja pikendada süsteemset poolväärtusaega, kuid tirzepatiidi kahe retseptori aktiivsus annab laiema metaboolse signaali.
Kuidas on semaglutiid ja tirzepatiid biokeemiliselt klassifitseeritud?
Semaglutiid on biokeemiliselt klassifitseeritud pika toimeajaga lipiiditud GLP-1 retseptori agonistpeptiidiks. Tirzepatiid on klassifitseeritud pika toimeajaga lipiiditud kahekordse inkretiiniretseptori agonistide peptiidina, täpsemalt GLP-1R/GIPR koagonistina.

Hielscher Ultrasonics toodab suure jõudlusega ultraheli homogenisaatoreid alates Lab kuni tööstuslik suurus.