سمگلوتاید لیپوزومی می تواند جهش بزرگ بعدی در انتقال داروی GLP-1 باشد
، کاترین هیلشر، منتشر شده در Hielscher اخبار
پپتیدهای GLP-1 مانند سمگلوتاید به یکی از تأثیرگذارترین درمان های پپتیدی دهه گذشته تبدیل شده اند و کاربرد بالینی گسترده ای در دیابت نوع ۲ و چاقی دارند. با این حال، با وجود موفقیت بالینی، چالش های فرمولاسیون و ساخت سمگلوتاید همچنان نماینده داروهای پپتیدی به طور کلی است: آن ها از نظر ساختاری شکننده، محافظت در برابر تخریب دشوار و به سختی تحویل آن ها از طریق مسیرهای غیرتهاجمی هستند. این محدودیت ها دلیل اصلی است که اکثر آگونیست های گیرنده GLP-1 هنوز به تزریق ها وابسته اند، حتی با وجود اینکه تقاضا برای ارائه خوراکی یا مناسب بیمار همچنان در حال افزایش است.
محدودیت های فرمولاسیون های فعلی خوراکی GLP-1
توسعه پپتیدهای خوراکی GLP-1 نشان داد که تحویل خوراکی از نظر فنی ممکن است، اما محدودیت های اصلی راهبردهای موجود را نیز آشکار کرد. حتی در یک محصول تأییدشده، سمگلوتاید خوراکی زیست دسترسی بسیار پایینی دارد که معمولا کمتر از ۱٪ است که نیازمند دوز بالاتر و افزایش هزینه، تغییرپذیری و پیچیدگی فرمولاسیون است. این محدودیت ها علاقه به سیستم های حامل را که می توانند داروهای پپتیدی را محافظت کنند و احتمالا جذب را بدون تکیه انحصاری بر تقویت کننده های نفوذ شیمیایی بهبود بخشند، افزایش داده است.
لیپوزوم ها به عنوان یک پلتفرم تحویل با بلوغ فنی
 در میان سیستم های تحویل مورد بررسی، کپسوله سازی لیپوزومی به دلیل بلوغ فنی و اهمیت دارویی اش برجسته است. لیپوزوم ها از دو لایه فسفولیپیدی تشکیل شده اند که شباهت زیادی به غشاهای زیستی دارند و سابقه طولانی در کاربرد بالینی در انکولوژی و بیماری های عفونی دارند. اهمیت آن ها برای درمان های پپتیدی در توانایی شان در محافظت فیزیکی از APIهای حساس در حالی است که اندازه، ترکیب و خواص سطحی قابل تنظیم را ارائه می دهند. با این حال، عملکرد لیپوزوم به شدت به توزیع اندازه، ساختار دو لایه، استراتژی بارگذاری و قابلیت تکرارپذیری تولید بستگی دارد – عواملی که عمدتا توسط فناوری فرآیند کنترل می شوند، نه صرفا ترکیب فرمولاسیون ها.
در میان سیستم های تحویل مورد بررسی، کپسوله سازی لیپوزومی به دلیل بلوغ فنی و اهمیت دارویی اش برجسته است. لیپوزوم ها از دو لایه فسفولیپیدی تشکیل شده اند که شباهت زیادی به غشاهای زیستی دارند و سابقه طولانی در کاربرد بالینی در انکولوژی و بیماری های عفونی دارند. اهمیت آن ها برای درمان های پپتیدی در توانایی شان در محافظت فیزیکی از APIهای حساس در حالی است که اندازه، ترکیب و خواص سطحی قابل تنظیم را ارائه می دهند. با این حال، عملکرد لیپوزوم به شدت به توزیع اندازه، ساختار دو لایه، استراتژی بارگذاری و قابلیت تکرارپذیری تولید بستگی دارد – عواملی که عمدتا توسط فناوری فرآیند کنترل می شوند، نه صرفا ترکیب فرمولاسیون ها.
چرا فرآوری اولتراسونیک بخش مرکزی تولید لیپوزوم است
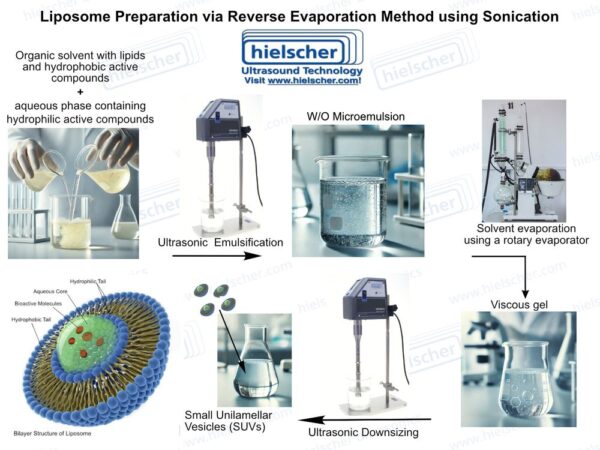
پردازش اولتراسونیک چندین چالش اصلی مرتبط با تولید لیپوزوم را برطرف می کند. اولتراسوند با شدت بالا کاویتاسیون صوتی در مایعات ایجاد می کند که نیروهای برشی موضعی و اثرات اختلاط میکرو را ایجاد می کند که می تواند تجمعات لیپیدی را تجزیه کرده و ساختارهای چندلایه ای را به وزیکول های کوچکتر و یکنواخت تر تبدیل کند. در ساخت لیپوزوم، سونوگرافی می تواند در هنگام تشکیل وزیکول یا به عنوان مرحله پس پردازش برای استانداردسازی اندازه ذرات و کیفیت پراکندگی به کار رود. این نقش دوگانه سونوگرافی را به ویژه در کنترل ویژگی های حیاتی کیفیت سیستم های لیپوزومی ارزشمند می کند.
سازگاری ساختاری سمگلوتاید با لایه های لیپیدی
پپتیدهای GLP-1 مانند سمگلوتاید یا تیرزپاتاید به ویژه برای حامل های مبتنی بر لیپید مناسب هستند زیرا یک پپتید خطی ساده نیستند. این مولکول دارای یک دم لیپیدی شیمیایی اصلاح شده است که تعامل با غشاهای لیپیدی را ترویج می کند. مطالعات تجربی با استفاده از سیستم های وزیکول نشان داده اند که سمگلوتاید و پپتیدهای مرتبط می توانند از طریق وارد کردن این دم لیپیدی با غشاهای وزیکول ارتباط برقرار کنند. اگرچه این یافته ها با استفاده از وزیکول های خارج سلولی مشتق شده از شیر به جای لیپوزوم های مصنوعی به دست آمده اند، مکانیزم زیرین به طور مستقیم قابل انتقال است. پپتیدهای لیپیدیت شده تمایل ذاتی به لایه های دوگانه فسفولیپیدی دارند که می تواند کارایی بارگذاری و پایداری فرمولاسیون را بدون نیاز به مزدوج سازی شیمیایی پیچیده بهبود بخشد.
شرایط فرآیند تعیین کننده کارایی کپسوله سازی است
یک بینش حیاتی از مطالعات اخیر مبتنی بر وزیکول این است که کارایی کپسوله سازی به شدت به روش بارگذاری و پردازش وابسته است. این موضوع پیامدهای مهمی برای توسعه دارو دارد: موفقیت یا شکست فرمولاسیون لیپوزوم پپتیدی اغلب بیشتر به نحوه تولید و فرآوری وزیکول ها بستگی دارد تا انتخاب لیپید. پردازش اولتراسونیک روشی قابل کنترل و تکرارپذیر برای تأثیرگذاری بر این پارامترها فراهم می کند که آن را به ویژه برای توسعه نظام مند فرمول بندی جذاب می سازد.
مقیاس پذیری به عنوان مزیت کلیدی پردازش اولتراسونیک
از دیدگاه تولید، یکی از مهم ترین مزایای سونوگرافی مقیاس پذیری آن است. برخلاف بسیاری از تکنیک های تولید نانوذرات که به شرایط دسته ای خاص هندسه متکی هستند، پردازش فراصوت می تواند با کنترل ورودی انرژی در واحد حجم مقیاس پذیر شود. این امکان را فراهم می کند که فرآیندهای توسعه یافته در مقیاس آزمایشگاهی به سیستم های آزمایشی و صنعتی با قابلیت مقایسه بالا منتقل شوند. برای تولیدکنندگان دارویی، این ویژگی از قابلیت تکرارپذیری، اعتبارسنجی و انتقال مؤثر فناوری در مراحل توسعه پشتیبانی می کند.
سونیکاسیون جریان پیوسته برای تولید صنعتی
مهم ترین پیاده سازی صنعتی پردازش لیپوزوم اولتراسونی، عملیات جریان پیوسته است. در سلول های صوتی جریان عبوری، پراکندگی لیپوزوم از یک حجم مشخص راکتور عبور می کند در حالی که اولتراسوند تحت فشار، دامنه و دمای کنترل شده اعمال می شود. این پیکربندی امکان کنترل دقیق بر زمان و مواجهه با انرژی محل سکونت را فراهم می کند. برای لیپوزوم های بارگذاری شده با پپتید، جایی که حساسیت حرارتی و یکپارچگی ساختاری حیاتی است، چنین کنترلی برای حفظ کیفیت محصول در مقیاس وسیع ضروری است.
ارتباط با درمان های نسل بعدی GLP-1 و پپتیدی
با پیشرفت درمان های GLP-1 به سمت پپتیدهای دو آگونیست و چندآگونیست، انتظار می رود پیچیدگی فرمولاسیون افزایش یابد. در عین حال، تقاضای بیماران برای روش های زایمان خوراکی یا کمتر تهاجمی همچنان در حال افزایش است. بنابراین پلتفرم های توزیع مبتنی بر حامل مقیاس پذیر از نظر استراتژیک اهمیت پیدا می کنند، نه تنها برای بهبود فارماکوکینتیک بلکه برای اطمینان از تولید قابل اعتماد داروهای پپتیدی جدید در مقیاس تجاری.
پرداختن به مانع بنیادی در تحویل پپتید خوراکی
دستگاه گوارش ذاتا نسبت به پپتیدها دشمن است و دسترسی زیستی پایین خوراکی حتی برای فرمولاسیون های پیشرفته مانعی اساسی باقی می ماند. کپسوله سازی لیپوزومی این چالش را از بین نمی برد، اما رویکردی مهندسی منطقی برای کاهش تخریب و کنترل نحوه تعامل پپتیدها با محیط های روده ای ارائه می دهد. وقتی با فناوری های پردازش مقیاس پذیر مانند اولتراسوند ترکیب شوند، سیستم های تحویل مبتنی بر لیپوزوم به امکان سنجی صنعتی نزدیک تر می شوند و محدود به آزمایش های آزمایشگاهی نیستند.
از توسعه آزمایشگاهی تا پیاده سازی صنعتی
 در جریان های کاری عملی توسعه، سیستم های اولتراسونیک هیلشر اغلب به عنوان پلتفرم مرجع برای پردازش لیپوزوم اولتراسونیک استفاده می شوند. در مقیاس آزمایشگاهی و توسعه فرمولاسیون ها، پروب های اولتراسونیک فشرده مانند UP200Ht و UP400St امکان پردازش کنترل شده در دسته های کوچک و بهینه سازی روش را فراهم می کنند. برای تولید صنعتی، سونیکاتورهای مجهز به راکتورهای جریان عبوری از عملکرد مستمر، چگالی توان بالا و مقیاس پذیری خطی پشتیبانی می کنند. این ویژگی ها با نیازهای محیط های تولید دارویی، از جمله کنترل فرآیند و قابلیت تکرار، همسو هستند.
در جریان های کاری عملی توسعه، سیستم های اولتراسونیک هیلشر اغلب به عنوان پلتفرم مرجع برای پردازش لیپوزوم اولتراسونیک استفاده می شوند. در مقیاس آزمایشگاهی و توسعه فرمولاسیون ها، پروب های اولتراسونیک فشرده مانند UP200Ht و UP400St امکان پردازش کنترل شده در دسته های کوچک و بهینه سازی روش را فراهم می کنند. برای تولید صنعتی، سونیکاتورهای مجهز به راکتورهای جریان عبوری از عملکرد مستمر، چگالی توان بالا و مقیاس پذیری خطی پشتیبانی می کنند. این ویژگی ها با نیازهای محیط های تولید دارویی، از جمله کنترل فرآیند و قابلیت تکرار، همسو هستند.
فراتر از سمگلوتاید: دیدگاه پلتفرم
در حالی که سمگلوتاید به عنوان یک ترکیب مدل بسیار مرتبط عمل می کند، پیامدهای کپسوله سازی لیپوزوم اولتراسونیک فراتر از یک API واحد است. همین منطق فرآیند برای سایر پپتیدهای لیپیداته، مزدوج پپتیدی ها و زیست شناسی های نوظهور نیز صدق می کند. با گسترش درمان های پپتیدی در بیماری های متابولیک، انکولوژی و ایمنی شناسی، فناوری های کپسوله سازی مقیاس پذیر احتمالا به عوامل تعیین کننده ای در تعیین اینکه کدام استراتژی های ارائه می توانند از مفهوم به واقعیت تجاری تبدیل شوند، تبدیل خواهند شد.
تغییر به سوی تحویل پپتید مهندسی شده توسط فرآیند
سمگلوتاید لیپوزومی کپسوله شده با اولتراسوند نشان دهنده تغییر گسترده تری در توسعه داروسازی است: از مفاهیم فرمولاسیون که عمدتا بر اساس منطق زیستی هدایت می شوند به سمت سیستم های تحویل مبتنی بر مهندسی فرآیند و قابلیت ساخت. در حوزه ای که بسیاری از فناوری های پپتید خوراکی در مقیاس پذیری شکست می خورند، پردازش لیپوزوم اولتراسونیک مسیری نسبتا مستقیم و از نظر فنی مقاوم از توسعه آزمایشگاهی تا تولید صنعتی ارائه می دهد.
ادبیات / منابع
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
پرسش و پاسخهای متداول
پپتیدهای GLP-1 چیستند؟
پپتیدهای GLP-1 داروهای پپتیدی تقلیدی اینکرتین هستند که گیرنده پپتید-۱ شبیه گلوکاگون (GLP-1R) را فعال می کنند؛ گیرنده ای کلیدی متابولیک که در ترشح انسولین وابسته به گلوکز، سرکوب آزادسازی گلوکاگون، تأخیر در تخلیه معده و تنظیم اشتها نقش دارد. پپتیدهای GLP-1 که به صورت بالینی استفاده می شوند (مانند سمگلوتاید) به صورت شیمیایی اصلاح شده اند تا در برابر تخریب آنزیمی مقاومت کنند و زمان گردش بیشتری نسبت به GLP-1 بومی داشته باشند.
تفاوت بین سمگلوتاید و تیرزپاتاید چیست؟
سمگلوتاید یک پپتید تک آگونیست است که به طور انتخابی گیرنده پپتید-۱ شبیه گلوکاگون (GLP-1R) را فعال می کند، در حالی که تیرزپاتاید یک آگونیست دوگانه است که هم گیرنده GLP-1 و هم گیرنده پلی پپتید وابسته به گلوکز (GIPR) را فعال می کند. از نظر بیوشیمیایی، تیرزپاتاید پپتیدی بزرگ تر و پیچیده تر است که عناصر توالی و دامنه های اتصال گیرنده آن ها برای درگیر کردن دو گیرنده اینکرتین بهینه شده اند، در حالی که سمگلوتاید به طور خاص برای فعال سازی GLP-1R با تمایل بالا مهندسی شده است. هر دو پپتید به صورت شیمیایی با بخش های لیپیدی اصلاح شده اند تا اتصال پروتئین پلاسما را افزایش داده و نیمه عمر سیستمیک را افزایش دهند، اما فعالیت گیرنده دوگانه تیرزپاتاید منجر به سیگنال دهی متابولیکی گسترده تر می شود.
سمگلوتاید و تیرزپاتاید چگونه به صورت بیوشیمیایی طبقه بندی می شوند؟
سمگلوتاید از نظر بیوشیمیایی به عنوان یک پپتید آگونیست گیرنده GLP-1 با اثر طولانی و لیپیده طبقه بندی می شود. تیرزپاتاید به عنوان یک پپتید آگونیست گیرنده دوگانه اینکرتین با اثر طولانی اثر و لیپیداته طبقه بندی می شود که به طور خاص یک کو-آگونیست GLP-1R/GIPR می باشد.

Hielscher مافوق صوت تولید کننده هموژنایزرهای مافوق صوت با کارایی بالا از ازمایشگاه ها تا اندازه صنعتی.