کپسوله سازی اولتراسونیک لیپوزوم پپتیدهای GLP-1: فناوری مقیاس پذیر برای تحویل خوراکی پپتید
سمگلوتاید و سایر پپتیدهای GLP-1 در حال تحول در مراقبت از دیابت و چاقی هستند، اما بیشتر داروهای پپتیدی هنوز نیاز به تزریق دارند زیرا تحویل خوراکی همچنان بسیار چالش برانگیز است. حتی سمگلوتاید خوراکی تأیید شده نیز زیست دسترسی را زیر ۱٪ نشان می دهد که نیاز به دوز و هزینه را افزایش می دهد. کپسوله سازی پپتیدهای GLP-1 در لیپوزوم ها می تواند این محدودیت ها را برطرف کند. بیاموزید چگونه تهیه لیپوزوم اولتراسونیک لیپوزوم های بارگذاری شده با پپتید GLP-1 را در داروخانه های ترکیبی و تولید داروسازی تسهیل می کند.
پپتیدهای لیپوزومی GLP-1
آگونیست های گیرنده GLP-1 مانند سمگلوتاید و پپتیدهای نسل بعدی اینکرتین مانند تیرزپاتاید، درمان دیابت نوع ۲ و چاقی را متحول کرده اند. با این حال، از نظر فرمولاسیون و ساخت، این APIها همچنان محدودیت کلاسیک داروهای پپتیدی را دارند: آن ها شکننده، به راحتی تجزیه می شوند و انتقال آن ها از طریق دستگاه گوارش دشوار است.
به همین دلیل است که بیشتر پپتیدهای GLP-1 همچنان قابل تزریق باقی می مانند، حتی اگر تحویل خوراکی موانع را برای بیماران به طور چشمگیری کاهش دهد. زایمان خوراکی معمولا راحتی، پایبندی و تمایل به شروع زودهنگام درمان را افزایش می دهد – به ویژه در بیماری های مزمن.
با این حال، تحویل خوراکی پپتید همچنان یکی از دشوارترین چالش ها در علم داروسازی است. حتی محصولات تأیید شده سماگلوتاید خوراکی نیز دسترسی زیستی بسیار پایینی دارند که نیازمند دوزهای بالا و استراتژی های دقیق فرمولاسیون است.
یکی از امیدبخش ترین رویکردهای فنی برای غلبه بر این محدودیت ها، کپسوله سازی لیپوزومی است که با پردازش اولتراسونیک با شدت بالا ترکیب می شود. لیپوزوم ها از APIهای پپتیدی محافظت می کنند، پایداری پراکندگی را بهبود می بخشند و می توانند برای اندازه های نانو مقیاس که برای نفوذ مخاط و تعامل روده ای اهمیت دارند، مهندسی شوند. سونیکاسیون روشی مقیاس پذیر و قابل تکرار برای تولید این لیپوزوم ها در حجم های صنعتی فراهم می کند.
چرا لیپوزوم ها بستری قوی برای پپتیدهای GLP-1 هستند
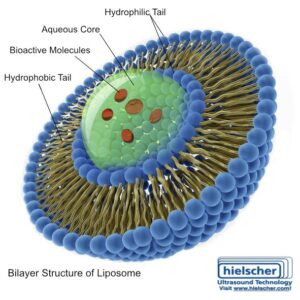 لیپوزوم ها وزیکول هایی هستند که توسط لایه های دوگانه فسفولیپیدی تشکیل شده اند و از نظر ترکیب مشابه غشاهای زیستی می باشند. این موضوع آن ها را ذاتا زیست سازگار و مناسب برای توسعه دارویی می کند. برای داروهای پپتیدی، لیپوزوم ها جذاب هستند زیرا می توانند API را به طور فیزیکی محافظت کنند و معماری فرمولاسیون را برای عملکرد تحویل تنظیم کنند.
لیپوزوم ها وزیکول هایی هستند که توسط لایه های دوگانه فسفولیپیدی تشکیل شده اند و از نظر ترکیب مشابه غشاهای زیستی می باشند. این موضوع آن ها را ذاتا زیست سازگار و مناسب برای توسعه دارویی می کند. برای داروهای پپتیدی، لیپوزوم ها جذاب هستند زیرا می توانند API را به طور فیزیکی محافظت کنند و معماری فرمولاسیون را برای عملکرد تحویل تنظیم کنند.
در زمینه پپتیدهای GLP-1، چالش اصلی نه تنها محافظت از پپتید در برابر اسید و آنزیم ها است، بلکه امکان جذب معنادار در سراسر سد روده ای است. این یک مشکل چندلایه است که شامل pH، تخریب آنزیمی، انتقال مخاط، نفوذپذیری اپیتلیال و مکانیزم های انتقال می شود.
ادبیات علمی به طور فزاینده ای از این ایده حمایت می کند که حامل های مبتنی بر وزیکول می توانند پایداری پپتیدی و تعامل آن ها با سیستم های روده ای را بهبود بخشند.
چرا سمگلوتاید برای کپسوله سازی لیپوزومی به ویژه جالب است
سمگلوتاید فقط یک پپتید نیست – این یک پپتید با اصلاح دم لیپیدی داخلی است. این یکی از دلایل اصلی رفتار متفاوت آن نسبت به بسیاری از APIهای پپتیدی دیگر در سیستم های لیپیدی است.
پپتیدهای GLP-1 مانند سمگلوتاید و تیرزپاتاید از طریق ورود دم لیپیدی به غشای وزیکول وارد وزیکول ها می شوند.
از دیدگاه مهندسی، این موضوع اهمیت دارد زیرا نشان می دهد سمگلوتاید از نظر ساختاری با لایه های دوگانه لیپیدی سازگار است، به این معنا که ممکن است بتوان بدون تغییرات شیمیایی بیش از حد، ارتباط پایدار و بارگذاری معنادار را به دست آورد.
همین منطق برای سایر APIهای پپتیدی لیپیددار و کانژوگات های پپتید-دارو نیز صدق می کند.
واقعیت تولید: لیپوزوم ها باید قابل تولید و مقیاس پذیر باشند
کپسوله سازی لیپوزوم در آزمایشگاه دشوار نیست. مشکل واقعی زمانی آغاز می شود که یک فرمول باید به روشی قابل تکرار و در مقیاس وسیع تولید شود.
تولید صنعتی لیپوزوم باید کنترل موارد زیر را داشته باشد:
- توزیع اندازه لیپوزوم
- پلی پراکندگی
- راندمان کپسوله سازی
- پایداری پراکندگی
- تکرارپذیری دسته به دسته
- سازگاری با پردازش استریل
- اعتبارسنجی فرآیند و مستندسازی
بسیاری از روش های رایج لیپوزوم (گردابی، هیدراتاسیون ساده، اکستروژن دستی) می توانند نتایج خوبی در بنچ تولید ایجاد کنند – اما وقتی به حجم پایلوت یا تولید منتقل می شوند، شکست می خورند.
اینجاست که پردازش اولتراسونیک به یک فناوری کلیدی تبدیل می شود.
کپسوله سازی اولتراسونیک لیپوزوم: اصل اصلی
سونوگرافی با شدت بالا انرژی مکانیکی را از طریق کاویتاسیون صوتی به مایع وارد می کند. کاویتاسیون تشکیل و فروپاشی حباب های میکروسکوپی است که نیروهای برشی موضعی و اثرات اختلاط میکرو را ایجاد می کند.
در پراکندگی های لیپیدی، این نیروها:
- میکروامولسیون ها را ایجاد کنید تا تشکیل لیپوزوم را آغاز کنید
- تجزیه تجمعات بزرگ لیپیدی
- کاهش ساختارهای چندلایه ای
- وزیکول های کوچکتر و یکنواخت تر تولید می کنند
- بهبود همگن سازی
- افزایش تکرارپذیری پراکندگی نهایی
بنابراین فرآوری اولتراسونیک به طور گسترده ای در تولید نانومواد، امولسیون سازی و پراکندگی استفاده می شود – و برای اندازه گیری نانو-لیپوزوم بسیار مناسب است.
برای لیپوزوم های پپتیدی GLP-1، سونوگرافی می تواند یا برای ایجاد لیپوزوم ها مستقیما در حین هیدراتاسیون و پراکندگی، یا به عنوان مرحله پس پردازش برای تصفیه اندازه وزیکول و بهبود یکنواختی استفاده شود.
چرا سونوگرافی به ویژه برای تولید لیپوزوم های دارویی ارزشمند است
مهم ترین دلیل استفاده صنعتی از اولتراسوند این است که می توان آن را با کنترل یک پارامتر فرآیند قابل اندازه گیری مقیاس بندی کرد: انرژی به ازای حجم.
به جای مقیاس بندی با “میکس بیشتر” یا “پردازش طولانی تر،” سیستم های فراصوت اجازه می دهند فرآیند به صورت زیر مقیاس بندی شود:
- افزایش توان اولتراسونیک
- افزایش دبی
- حفظ همان انرژی ورودی در هر میلی لیتر
- استفاده از راکتورهای جریان پیوسته
- شماره گذاری به صورت موازی
این باعث می شود فرآیند بسیار قابل انتقال از R باشد&D به تولید.
از نظر عملی، این بدان معناست که فرآیند لیپوزوم توسعه یافته روی یک سیستم کوچک می تواند به سیستم های بزرگ تر منتقل شود در حالی که شرایط فرآیند معادل حفظ می شود، که دقیقا همان چیزی است که تولید دارو نیاز دارد.
تأثیر بر پپتیدهای GLP-1: به سوی دسترسی زیستی بهتر خوراکی
زایمان خوراکی هدف بلندمدت بسیاری از فرمولاسیون های پپتیدی GLP-1 است. دلیل آن ساده است: اگر دسترسی زیستی خوراکی بهبود یابد، کل درمان برای بیماران آسان تر می شود.
مطالب آپلود شده شما محدودیت فعلی را برجسته می کند: سمگلوتاید خوراکی ممکن است، اما زیست دسترسی همچنان پایین است (کمتر از ۱٪).
کپسوله سازی لیپوزوم تضمینی برای دسترسی زیستی دهانی بالا نیست، اما چندین گلوگاه حیاتی را به طور همزمان برطرف می کند:
- این ماده می تواند به طور فیزیکی پپتید را در برابر تخریب محافظت کند.
- این دستگاه می تواند حامل های نانومقیاس با ویژگی هایی متناسب با نفوذ مخاط ایجاد کند.
- می توان آن را با لیگاندهای سطحی برای مکانیزم های انتقال فعال فعال کرد.
- این می تواند سازگاری و قابلیت بازتولید فرم API ارائه شده را بهبود بخشد.
به ویژه برای سمگلوتاید، ارتباط غشا از طریق دم لیپیدی مکانیزم اضافی ای فراهم می کند که ممکن است پپتید را در سیستم های لیپیدی تثبیت کند.
پردازش اولتراسونیک امکان تولید مداوم و صنعتی لیپوزوم را فراهم می کند
در تولید صنعتی، فرآوری پیوسته اغلب ترجیح داده می شود زیرا بهبود می یابد:
- توان
- تکرارپذیری
- کنترل فرآیند
- ادغام در جریان های کاری تولید استریل
سیستم های جریان اولتراسونیک برای این منظور ایده آل هستند. پراکندگی لیپوزوم از طریق یک سلول جریان تحت فشار پمپ می شود که در آن اولتراسوند تحت شرایط کنترل شده اعمال می شود. دما، فشار و زمان ماندگاری قابل کنترل است که برای فرمولاسیون پپتیدی ضروری است.
این امکان را فراهم می کند تا جریان های کاری مقیاس پذیر با اندازه گیری نانو و کپسوله سازی انجام شود که بسیار به نیازهای GMP نزدیک تر از بسیاری از روش های صرفا آزمایشگاهی است.
اولتراسونیک هیلشر: سیستم های آزمایشگاهی تا صنعتی برای کپسوله سازی لیپوزوم

شرکت Hielscher Ultrasonics سیستم های اولتراسونیک را ارائه می دهد که با مسیر واقعی توسعه فرمولاسیون های پپتید لیپوزومی مطابقت دارند.
در مقیاس آزمایشگاهی، UP400St به طور گسترده برای غربالگری فرمولاسیون ها، توسعه فرآیندها و آماده سازی لیپوزوم در مقیاس ترکیبی استفاده می شود.
در مقیاس تولید، UIP2000hdT و UIP4000hdT برای چرخه های کاری صنعتی طراحی شده اند و می توانند با سلول های صوتی جریان عبوری برای پردازش پیوسته یکپارچه شوند.
این ترکیب به ویژه برای تولید لیپوزوم دارویی اهمیت دارد زیرا از موارد زیر پشتیبانی می کند:
- قابلیت بازتولید فرآیند
- مقیاس پذیری خطی
- تولید جریان پیوسته
- پردازش اولتراسونیک با توان بالا در شرایط کنترل شده

Sonicator UIP1000hdT با سلول جریان شیشه ای برای تولید لیپوزوم ها.
در یک نگاه – چرا فرمولاسیون اولتراسونیک لیپوزوم پپتیدهای GLP-1
کپسوله سازی لیپوزوم اولتراسونیک یکی از پیشرفته ترین و صنعتی ترین روش ها برای تولید لیپوزوم های بارگذاری شده با پپتید است. برای پپتیدهای GLP-1 مانند سمگلوتاید و تیرزپاتید، این رویکرد به ویژه اهمیت دارد زیرا این APIها از نظر ساختاری با غشاهای لیپیدی سازگار هستند و می توانند از راهبردهای حفاظت و انتقال مبتنی بر وزیکول بهره مند شوند.
مهم تر از همه، سونوگرافی صرفا یک روش آزمایشگاهی نیست – این یک فناوری فرآیندی مقیاس پذیر است. با کنترل ورودی انرژی به ازای حجم و استفاده از سلول های صوتی جریان عبوری، پردازش اولتراسونیک می تواند از توسعه در مقیاس آزمایشگاهی به تولید آزمایشی و صنعتی کامل منتقل شود.
با ادامه حرکت صنعت داروسازی به سمت درمان های پپتیدی – و با افزایش تقاضا برای مسیرهای تحویل مناسب برای بیماران – تولید لیپوزوم اولتراسونیک نقش مرکزی فزاینده ای در امکان پذیر ساختن نسل بعدی فرمولاسیون های GLP-1 ایفا خواهد کرد.
جدول زیر به شما نشانه ای از ظرفیت پردازش تقریبی مافوق صوت ما می دهد:
| حجم دسته ای | نرخ جریان | دستگاه های توصیه شده |
|---|---|---|
| 0.5 تا 1.5 میلی لیتر | ن.ا. | VialTweeter(ویال گروهی) |
| 1 تا 500 میلی لیتر | 10 تا 200 میلی لیتر در دقیقه | UP100H |
| 10 تا 2000 میلی لیتر | 20 تا 400 میلی لیتر در دقیقه | تا 200 هرتز، UP400St |
| 0.1 تا 20 لیتر | 0.2 تا 4 لیتر در دقیقه | UIP2000hdT |
| 10 تا 100 لیتر | 2 تا 10 لیتر در دقیقه | UIP4000hdT |
| 15 تا 150 لیتر | 3 تا 15 لیتر در دقیقه | UIP6000hdT |
| ن.ا. | 10 تا 100 لیتر در دقیقه | UIP16000hdT |
| ن.ا. | بزرگتر | خوشه ای از UIP16000hdT |
طراحی، ساخت و مشاوره – کیفیت ساخت آلمان
مافوق صوت Hielscher به خوبی برای بالاترین کیفیت و استانداردهای طراحی خود را شناخته شده. استحکام و بهره برداری آسان اجازه می دهد تا ادغام صاف از ultrasonicators ما به امکانات صنعتی. شرایط خشن و محیط های خواستار به راحتی توسط مافوق صوت Hielscher رسیده.
Hielscher اولتراسونیک یک شرکت دارای گواهینامه ISO است و تاکید ویژه ای بر مافوق صوت با کارایی بالا با ویژگی های دولت از هنر فن آوری و کاربر پسند قرار داده است. البته، مافوق صوت Hielscher مطابق با CE و دیدار با الزامات UL، CSA و RoHs.
ادبیات / منابع
- Martyna Truszkowska; Ahmad Saleh; Melanie Lena Eber; Gergely Kali; Andreas Bernkop-Schnürch (2025): Addressing the polycation dilemma in drug delivery: charge-converting liposomes. Journal of Materials Chemistry B 2025, 13, 9100-9111.
- Pop, R.; Nistor, M.; Socaciu, C.; Cenariu, M.; Tăbăran, F.; Rugină, D.; Pintea, A.; Socaciu, M.A. (2025): Distinct In Vitro Effects of Liposomal and Nanostructured Lipid Nanoformulations with Entrapped Acidic and Neutral Doxorubicin on B16-F10 Melanoma and Walker 256 Carcinoma Cells. Pharmaceutics 2025, 17, 904.
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
پرسش و پاسخهای متداول
نقش امولسیفیکاسیون اولتراسونیک در تشکیل لیپوزوم چیست؟
امولسیون سازی فراصوت فاز آبی و لیپیدها انرژی مکانیکی لازم برای پراکندگی دقیق لیپیدها در آب و هدایت خودتجمع آن ها به ساختارهای دو لایه بسته را فراهم می کند. کاویتاسیون صوتی تولید شده توسط اولتراسوند، نیروهای شدید میکرومیکس و برشی ایجاد می کند که فازهای لیپیدی را تکه تکه می کند، مولکول های لیپید را به طور یکنواخت هیدراته می کند و قطعات پراکنده لیپیدی را به وزیکول های لیپوزومی تبدیل می کند. این امر تشکیل سریع وزیکول ها، کاهش ساختارهای چندلایه ای و تولید لیپوزوم های کوچکتر و یکنواخت تر با بازتولیدپذیری و پایداری بهتر را ترویج می کند.
چه چیزهایی باید درباره فرمولاسیون GLP-1 بدانم؟
پپتیدهای GLP-1 داروهای بسیار مؤثری هستند، اما بیشتر آن ها به دلیل تخریب دستگاه گوارش و موانع جذب قابل تزریق باقی می مانند.
سماگلوتاید خوراکی وجود دارد، اما میزان دسترسی زیستی گزارش شده زیر ۱٪ باقی می ماند.
سمگلوتاید و تیرزپاتاید را می توان در سیستم های وزیکول بارگذاری کرد و کارایی بارگذاری به شدت به روش پردازش بستگی دارد.
سماگلوتاید ممکن است از طریق دم لیپیدی خود با غشاهای لیپیدی ارتباط برقرار کند و از سازگاری وزیکول/لیپوزوم حمایت کند.
کاویتاسیون اولتراسونیک امکان همگن سازی نانوزامی و پراکندگی قابل بازتولید لیپوزوم را فراهم می کند.
سونوگرافی به صورت خطی از طریق کنترل انرژی بر حجم و پردازش جریان پیوسته مقیاس می شود.
سیستم های هیلشر از کل روند کاری پشتیبانی می کنند:
- UP400St (مقیاس آزمایشگاهی و ترکیبی)
- UIP2000hdT / UIP4000hdT + سلول های جریان (تولید دارویی صنعتی)
پپتیدهای GLP-1 چیستند؟
پپتیدهای GLP-1 آگونیست های گیرنده اینکرتین مبتنی بر پپتید هستند که فعالیت زیستی پپتید-۱ شبه گلوکاگون (GLP-1) را تقلید یا تقویت می کنند؛ هورمونی روده در ترشح انسولین وابسته به گلوکز، سرکوب ترشح گلوکاگون و تنظیم تخلیه و اشتهای معده نقش دارد. داروهای GLP-1 که به صورت بالینی استفاده می شوند (مانند سمگلوتاید) به صورت شیمیایی اصلاح شده اند تا در برابر تخریب آنزیمی مقاومت کرده و نیمه عمر سیستمیک طولانی داشته باشند.
پپتیدهای GLP-1 به طور معمول چگونه تجویز می شوند؟
بیشتر پپتیدهای GLP-1 به صورت تزریق زیرجلدی تزریق می شوند زیرا پپتیدها در دستگاه گوارش ناپایدار هستند و نفوذپذیری روده بسیار پایینی دارند. مصرف خوراکی برای سمگلوتاید با استفاده از استراتژی های تخصصی فرمولاسیون حاصل شده است، اما زیست دسترسی خوراکی همچنان پایین است (حدود ۰.۴٪ تا ۱٪ گزارش شده است).
مزایای تجویز خوراکی لیپوزوم های پپتیدی GLP-1 چیست؟
لیپوزوم های خوراکی پپتیدی GLP-1 می توانند راحتی و پایبندی بیماران را با حذف تزریق ها افزایش دهند و در عین حال جذب مؤثر را با محافظت از پپتیدها در برابر تخریب اسیدی و آنزیمی و بهبود انتقال از طریق مخاط و موانع اپیتلیال افزایش دهند. بهبود دسترسی زیستی خوراکی می تواند بار دوز را کاهش دهد، فشار هزینه را کاهش دهد و موانع شروع و حفظ درمان پپتیدی بلندمدت را کاهش دهد.

Hielscher مافوق صوت تولید کننده هموژنایزرهای مافوق صوت با کارایی بالا از ازمایشگاه ها تا اندازه صنعتی.



