Ліпосомальний семаглютид може стати наступним великим стрибком у доставці ліків GLP-1
, Катрін Хілшеропублікований в Hielscher News
Пептиди GLP-1, такі як семаглютид, стали одними з найвпливовіших пептидних терапевтичних засобів останнього десятиліття з широким клінічним застосуванням при діабеті 2 типу та ожирінні. Проте, незважаючи на його клінічний успіх, проблеми з розробкою та виробництвом семаглютиду залишаються типовими для пептидних препаратів загалом: вони структурно крихкі, їх важко захистити від деградації, і, як відомо, їх важко доставляти неінвазивними шляхами. Ці обмеження є основною причиною того, що більшість агоністів рецепторів GLP-1 все ще покладаються на ін'єкції, навіть незважаючи на те, що попит на пероральну або зручну для пацієнта доставку продовжує зростати.
Обмеження поточних пероральних препаратів GLP-1
Розробка пероральних пептидів GLP-1 продемонструвала, що пероральна доставка є технічно можливою, але вона також виявила основні обмеження існуючих стратегій. Навіть у схваленому продукті пероральний семаглютид має дуже низьку біодоступність, як правило, нижче 1%, що вимагає більш високого дозування і сприяє підвищенню вартості, варіабельності та складності формуляції. Ці обмеження посилили інтерес до систем на основі носіїв, які можуть захистити пептидні препарати і потенційно покращити абсорбцію, не покладаючись виключно на хімічні підсилювачі проникнення.
Ліпосоми як технічно зріла платформа для доставки
 Серед досліджуваних систем доставки ліпосомальна інкапсуляція виділяється своєю технічною зрілістю та фармацевтичною актуальністю. Ліпосоми складаються з фосфоліпідних шарів, які дуже нагадують біологічні мембрани і мають довгу історію клінічного застосування в онкології та інфекційних захворюваннях. Їх актуальність для пептидної терапії полягає в здатності фізично захищати чутливі АФІ, пропонуючи при цьому регульований розмір, склад і властивості поверхні. Однак ефективність ліпосом сильно залежить від розподілу за розмірами, структури бішару, стратегії завантаження та відтворюваності виробництва. – фактори, які визначаються насамперед технологією процесу, а не лише складом рецептури.
Серед досліджуваних систем доставки ліпосомальна інкапсуляція виділяється своєю технічною зрілістю та фармацевтичною актуальністю. Ліпосоми складаються з фосфоліпідних шарів, які дуже нагадують біологічні мембрани і мають довгу історію клінічного застосування в онкології та інфекційних захворюваннях. Їх актуальність для пептидної терапії полягає в здатності фізично захищати чутливі АФІ, пропонуючи при цьому регульований розмір, склад і властивості поверхні. Однак ефективність ліпосом сильно залежить від розподілу за розмірами, структури бішару, стратегії завантаження та відтворюваності виробництва. – фактори, які визначаються насамперед технологією процесу, а не лише складом рецептури.
Чому ультразвукова обробка є центральною для виробництва ліпосом
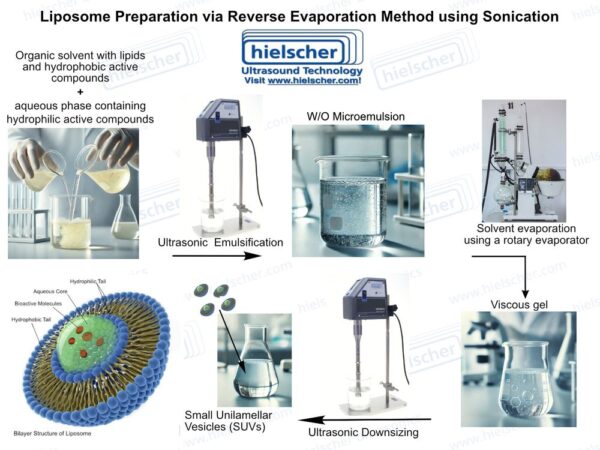
Ультразвукова обробка вирішує кілька основних проблем, пов'язаних з виробництвом ліпосом. Високоінтенсивний ультразвук генерує акустичну кавітацію в рідинах, створюючи локалізовані сили зсуву і ефекти мікроперемішування, які можуть руйнувати ліпідні агрегати і перетворювати багатошарові структури в менші, більш однорідні везикули. У виробництві ліпосом ультразвук може застосовуватися під час формування везикул або як етап пост-обробки для стандартизації розміру частинок і якості дисперсії. Ця подвійна роль робить ультразвук особливо цінним у контролі критичних атрибутів якості ліпосомальних систем.
Структурна сумісність семаглутиду з ліпідними шарами
Пептиди GLP-1, такі як семаглютид або тирзепатид, особливо добре підходять для ліпідних носіїв, оскільки вони не є простими лінійними пептидами. Молекула містить хімічно модифікований ліпідний хвіст, який сприяє взаємодії з ліпідними мембранами. Експериментальні дослідження з використанням везикулярних систем показали, що семаглютид і споріднені пептиди можуть асоціюватися з мембранами везикул завдяки вставці цього ліпідного хвоста. Хоча ці результати були отримані з використанням позаклітинних везикул молочного походження, а не синтетичних ліпосом, механізм, що лежить в їх основі, може бути безпосередньо перенесений. Ліпідні пептиди мають вроджену спорідненість до фосфоліпідних бішарів, що може підвищити ефективність завантаження та стабільність формуляції, не вимагаючи складної хімічної кон'югації.
Умови процесу визначають ефективність інкапсуляції
Важливим висновком останніх досліджень на основі везикул є те, що ефективність інкапсуляції сильно залежить від способу завантаження та обробки. Це має важливі наслідки для фармацевтичної розробки: успіх або невдача пептидних ліпосом часто залежить не стільки від вибору ліпіду, скільки від того, як виробляються і обробляються везикули. Ультразвукова обробка забезпечує контрольований і відтворюваний засіб впливу на ці параметри, що робить її особливо привабливою для систематичної розробки формулювань.
Масштабованість як ключова перевага ультразвукової обробки
З точки зору виробництва, однією з найважливіших переваг ультразвуку є його масштабованість. На відміну від багатьох методів виробництва наночастинок, які покладаються на специфічні геометричні умови партії, ультразвукову обробку можна масштабувати, контролюючи вхідну енергію на одиницю об'єму. Це дозволяє переносити процеси, розроблені в лабораторних масштабах, на пілотні та промислові системи з високою порівнянністю. Для фармацевтичних виробників ця характеристика підтримує відтворюваність, валідацію та ефективну передачу технологій на всіх етапах розробки.
Безперервна ультразвукова обробка потоку для промислового виробництва
Найбільш промислово релевантною реалізацією ультразвукової обробки ліпосом є безперервний потік. У прохідних ультразвукових комірках дисперсії ліпосом проходять через певний об'єм реактора, в той час як ультразвук подається під контрольованим тиском, амплітудою і температурою. Ця конфігурація дозволяє точно контролювати час перебування та енергетичний вплив. Для навантажених пептидами ліпосом, де термочутливість і структурна цілісність є критично важливими, такий контроль є необхідним для підтримки якості продукту в масштабі.
Актуальність для наступного покоління GLP-1 та пептидних терапевтичних засобів
Очікується, що в міру того, як терапія GLP-1 розвиватиметься в напрямку використання пептидів з подвійним та мультиагоністичним ефектом, складність формуляцій буде зростати. У той же час, попит пацієнтів на пероральні або менш інвазивні шляхи доставки продовжує зростати. Масштабовані платформи доставки на основі носіїв стають стратегічно важливими не тільки для покращення фармакокінетики, але й для забезпечення надійного виробництва нових пептидних препаратів у комерційних масштабах.
Усунення основного бар'єру для пероральної доставки пептидів
Шлунково-кишковий тракт за своєю природою є ворожим до пептидів, а низька біодоступність при пероральному застосуванні залишається фундаментальним бар'єром навіть для вдосконалених формулювань. Ліпосомальна інкапсуляція не усуває цю проблему, але забезпечує раціональний інженерний підхід для зменшення деградації та контролю взаємодії пептидів з кишковим середовищем. У поєднанні з масштабованими технологіями обробки, такими як ультразвук, системи доставки на основі ліпосом наближаються до промислової доцільності, а не залишаються обмеженими лабораторними експериментами.
Від лабораторних розробок до промислового впровадження
 У практичних робочих процесах розробки системи Hielscher Ultrasonics часто використовуються як еталонні платформи для ультразвукової обробки ліпосом. У лабораторних умовах і при розробці рецептур компактні ультразвукові датчики, такі як UP200Ht і UP400St, дозволяють проводити контрольовану обробку малих партій і оптимізувати методи. Для промислового виробництва сокатори, оснащені проточними реакторами, підтримують безперервну роботу, високу щільність потужності та лінійне масштабування. Ці характеристики відповідають вимогам фармацевтичного виробництва, включаючи контроль процесу і відтворюваність.
У практичних робочих процесах розробки системи Hielscher Ultrasonics часто використовуються як еталонні платформи для ультразвукової обробки ліпосом. У лабораторних умовах і при розробці рецептур компактні ультразвукові датчики, такі як UP200Ht і UP400St, дозволяють проводити контрольовану обробку малих партій і оптимізувати методи. Для промислового виробництва сокатори, оснащені проточними реакторами, підтримують безперервну роботу, високу щільність потужності та лінійне масштабування. Ці характеристики відповідають вимогам фармацевтичного виробництва, включаючи контроль процесу і відтворюваність.
Поза межами семаглутиди: Перспектива платформи
Хоча семаглютид служить дуже важливою модельною сполукою, наслідки інкапсуляції ультразвукових ліпосом виходять за рамки одного АФІ. Така ж логіка процесу застосовується до інших ліпідних пептидів, пептидних кон'югатів та нових біологічних препаратів. Оскільки пептидні терапевтичні засоби поширюються на метаболічні захворювання, онкологію та імунологію, масштабовані технології інкапсуляції, ймовірно, стануть вирішальними факторами у визначенні того, які стратегії доставки можуть перейти від концепції до комерційної реальності.
Перехід до технологічної доставки пептидів
Інкапсульований ультразвуком ліпосомальний семаглютид ілюструє ширший зсув у фармацевтичній розробці: від концепцій формулювання, зумовлених насамперед біологічним обґрунтуванням, до систем доставки, заснованих на технологічній інженерії та технологічності. У сфері, де багато пероральних пептидних технологій зазнають невдачі під час масштабування, ультразвукова обробка ліпосом пропонує порівняно прямий і технічно надійний шлях від лабораторних розробок до промислового виробництва.
Література / Список літератури
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
Поширені запитання
Що таке пептиди GLP-1?
Пептиди GLP-1 - це інкретин-міметичні пептидні препарати, які активують рецептор глюкагоноподібного пептиду-1 (GLP-1R), ключовий метаболічний рецептор, що бере участь у глюкозозалежній секреції інсуліну, пригніченні вивільнення глюкагону, затримці випорожнення шлунка та регуляції апетиту. Клінічно використовувані пептиди GLP-1 (наприклад, семаглютид) хімічно модифіковані, щоб протистояти ферментативній деградації і досягти більш тривалого часу циркуляції порівняно з нативним GLP-1.
У чому різниця між семаглутидом і тирзепатидом?
Семаглютид - це пептид з одним агоністом, який селективно активує рецептор глюкагоноподібного пептиду-1 (GLP-1R), тоді як тирзепатид є подвійним агоністом, який активує як рецептор GLP-1, так і глюкозозалежний рецептор інсулінотропного поліпептиду (GIPR). Біохімічно тирзепатід є більшим і складнішим пептидом з елементами послідовності та рецептор-зв'язуючими доменами, оптимізованими для взаємодії з двома інкретиновими рецепторами, тоді як семаглютид розроблений спеціально для високоафінної активації GLP-1R. Обидва пептиди хімічно модифіковані ліпідними фрагментами для збільшення зв'язування з білками плазми та подовження системного періоду напіввиведення, але подвійна рецепторна активність тирзепатиду призводить до ширшої метаболічної сигналізації.
Як біохімічно класифікуються семаглутид і тирзепатид?
Семаглютид біохімічно класифікується як ліпідний пептид-агоніст рецептора GLP-1 тривалої дії. Тірзепатід класифікується як ліпідний пептид-агоніст подвійного інкретинового рецептора тривалої дії, а саме як коагоніст GLP-1R/GIPR.

Hielscher Ultrasonics виробляє високоефективні ультразвукові гомогенізатори з Лабораторії до промислові розміри.