ლიპოსომული სემაგლუტიდი შესაძლოა GLP-1 წამლის მიწოდების შემდეგი დიდი ნახტომი იყოს
, კატრინ ჰილშერი, გამოქვეყნდა Hielscher News-ში
GLP-1 პეპტიდები, როგორიცაა სემაგლუტიდი, ბოლო ათწლეულის ერთ-ერთ ყველაზე გავლენიან პეპტიდურ თერაპიულ საშუალებად იქცა, რომელიც ფართო კლინიკურ გამოყენებას იჩენს მე-2 ტიპის დიაბეტისა და სიმსუქნის სამკურნალოდ. თუმცა, კლინიკური წარმატების მიუხედავად, სემაგლუტიდის ფორმულირებისა და წარმოების სირთულეები ზოგადად პეპტიდური პრეპარატების წარმომადგენელია: ისინი სტრუქტურულად მყიფეა, ძნელია მათი დაცვა დეგრადაციისგან და ცნობილია მათი არაინვაზიური გზით მიწოდება. ეს შეზღუდვები არის მთავარი მიზეზი, რის გამოც GLP-1 რეცეპტორების აგონისტების უმეტესობა კვლავ ინექციებზეა დამოკიდებული, მაშინაც კი, როდესაც პერორალური ან პაციენტისთვის მოსახერხებელი მიწოდების მოთხოვნა კვლავ იზრდება.
მიმდინარე პერორალური GLP-1 ფორმულირებების შეზღუდვები
ორალური GLP-1 პეპტიდების შემუშავებამ აჩვენა, რომ ორალური მიღება ტექნიკურად შესაძლებელია, მაგრამ ასევე გამოავლინა არსებული სტრატეგიების ძირითადი შეზღუდვები. დამტკიცებულ პროდუქტშიც კი, ორალური სემაგლუტიდი ავლენს ძალიან დაბალ ბიოშეღწევადობას, როგორც წესი, 1%-ზე ნაკლებს, რაც მოითხოვს უფრო მაღალ დოზირებას და ხელს უწყობს ფასს, ცვალებადობას და ფორმულირების სირთულეს. ამ შეზღუდვებმა გააძლიერა ინტერესი მატარებელზე დაფუძნებული სისტემების მიმართ, რომლებსაც შეუძლიათ დაიცვან პეპტიდური პრეპარატები და პოტენციურად გააუმჯობესონ შეწოვა მხოლოდ ქიმიური შეღწევადობის გამაძლიერებლებზე დაყრდნობის გარეშე.
ლიპოსომები, როგორც ტექნიკურად მომწიფებული მიწოდების პლატფორმა
 კვლევის პროცესში მყოფ მიწოდების სისტემებს შორის, ლიპოსომური ინკაფსულაცია გამოირჩევა თავისი ტექნიკური სიმწიფითა და ფარმაცევტული შესაბამისობით. ლიპოსომები შედგება ფოსფოლიპიდური ორმაგი შრეებისგან, რომლებიც ძალიან ჰგავს ბიოლოგიურ მემბრანებს და აქვთ ონკოლოგიასა და ინფექციურ დაავადებებში კლინიკური გამოყენების ხანგრძლივი ისტორია. მათი შესაბამისობა პეპტიდური თერაპიისთვის მდგომარეობს მგრძნობიარე API-ების ფიზიკურად დაცვის უნარში, ამავდროულად, ზომის, შემადგენლობისა და ზედაპირის თვისებების რეგულირების შეთავაზებით. თუმცა, ლიპოსომური მუშაობა მნიშვნელოვნად არის დამოკიდებული ზომის განაწილებაზე, ორმაგი შრის სტრუქტურაზე, დატვირთვის სტრატეგიასა და წარმოების რეპროდუცირებადობაზე. – ფაქტორები, რომლებიც ძირითადად განისაზღვრება პროცესის ტექნოლოგიით და არა მხოლოდ ფორმულირების შემადგენლობით.
კვლევის პროცესში მყოფ მიწოდების სისტემებს შორის, ლიპოსომური ინკაფსულაცია გამოირჩევა თავისი ტექნიკური სიმწიფითა და ფარმაცევტული შესაბამისობით. ლიპოსომები შედგება ფოსფოლიპიდური ორმაგი შრეებისგან, რომლებიც ძალიან ჰგავს ბიოლოგიურ მემბრანებს და აქვთ ონკოლოგიასა და ინფექციურ დაავადებებში კლინიკური გამოყენების ხანგრძლივი ისტორია. მათი შესაბამისობა პეპტიდური თერაპიისთვის მდგომარეობს მგრძნობიარე API-ების ფიზიკურად დაცვის უნარში, ამავდროულად, ზომის, შემადგენლობისა და ზედაპირის თვისებების რეგულირების შეთავაზებით. თუმცა, ლიპოსომური მუშაობა მნიშვნელოვნად არის დამოკიდებული ზომის განაწილებაზე, ორმაგი შრის სტრუქტურაზე, დატვირთვის სტრატეგიასა და წარმოების რეპროდუცირებადობაზე. – ფაქტორები, რომლებიც ძირითადად განისაზღვრება პროცესის ტექნოლოგიით და არა მხოლოდ ფორმულირების შემადგენლობით.
რატომ არის ულტრაბგერითი დამუშავება ლიპოსომის წარმოების ცენტრში
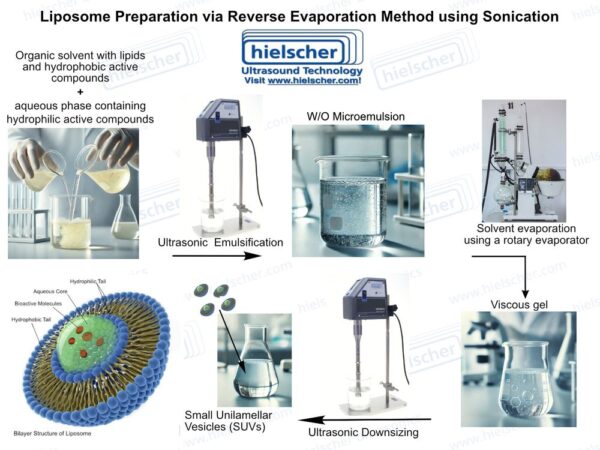
ულტრაბგერითი დამუშავება ლიპოსომების წარმოებასთან დაკავშირებულ რამდენიმე ძირითად გამოწვევას აგვარებს. მაღალი ინტენსივობის ულტრაბგერა სითხეებში აკუსტიკურ კავიტაციას წარმოქმნის, რაც ლოკალიზებულ ძვრის ძალებსა და მიკროშერევის ეფექტებს იწვევს, რომლებსაც შეუძლიათ ლიპიდური აგრეგატების დაშლა და მრავალშრიანი სტრუქტურების უფრო პატარა, უფრო ერთგვაროვან ვეზიკულებად გარდაქმნა. ლიპოსომების წარმოებაში ულტრაბგერის გამოყენება შესაძლებელია ვეზიკულების ფორმირების დროს ან დამუშავების შემდგომ ეტაპზე ნაწილაკების ზომისა და დისპერსიის ხარისხის სტანდარტიზაციის მიზნით. ეს ორმაგი როლი ულტრაბგერას განსაკუთრებით ღირებულს ხდის ლიპოსომური სისტემების კრიტიკული ხარისხის ატრიბუტების კონტროლში.
სემაგლუტიდის სტრუქტურული თავსებადობა ლიპიდურ ბიშრეებთან
GLP-1 პეპტიდები, როგორიცაა სემაგლუტიდი ან ტირზეპატიდი, განსაკუთრებით კარგად შეეფერება ლიპიდურ მატარებლებს, რადგან ის არ არის მარტივი ხაზოვანი პეპტიდი. მოლეკულა შეიცავს ქიმიურად მოდიფიცირებულ ლიპიდურ კუდს, რომელიც ხელს უწყობს ლიპიდურ მემბრანებთან ურთიერთქმედებას. ვეზიკულური სისტემების გამოყენებით ჩატარებულმა ექსპერიმენტულმა კვლევებმა აჩვენა, რომ სემაგლუტიდს და მასთან დაკავშირებულ პეპტიდებს შეუძლიათ ვეზიკულური მემბრანების შეერთება ამ ლიპიდური კუდის ჩასმის გზით. მიუხედავად იმისა, რომ ეს დასკვნები მიღებული იქნა რძისგან მიღებული უჯრედგარე ვეზიკულების გამოყენებით და არა სინთეზური ლიპოსომების გამოყენებით, ძირითადი მექანიზმი პირდაპირ გადაცემადია. ლიპიდირებულ პეპტიდებს აქვთ თანდაყოლილი აფინურობა ფოსფოლიპიდური ორმაგი შრეების მიმართ, რამაც შეიძლება გააუმჯობესოს დატვირთვის ეფექტურობა და ფორმულირების სტაბილურობა რთული ქიმიური კონიუგაციის გარეშე.
პროცესის პირობები განსაზღვრავს კაფსულაციის ეფექტურობას
ვეზიკულებზე დაფუძნებული ბოლოდროინდელი კვლევებიდან გამომდინარე მნიშვნელოვანი დასკვნა ის არის, რომ ინკაფსულაციის ეფექტურობა დიდად არის დამოკიდებული ჩატვირთვისა და დამუშავების მეთოდზე. ამას მნიშვნელოვანი გავლენა აქვს ფარმაცევტული განვითარებისთვის: პეპტიდური ლიპოსომის ფორმულირების წარმატება ან წარუმატებლობა ხშირად ნაკლებად არის დამოკიდებული ლიპიდის არჩევანზე და უფრო მეტად იმაზე, თუ როგორ წარმოიქმნება და დამუშავდება ვეზიკულები. ულტრაბგერითი დამუშავება უზრუნველყოფს ამ პარამეტრებზე გავლენის კონტროლირებად და რეპროდუცირებად საშუალებას, რაც მას განსაკუთრებით მიმზიდველს ხდის ფორმულირების სისტემატური შემუშავებისთვის.
მასშტაბირება, როგორც ულტრაბგერითი დამუშავების ძირითადი უპირატესობა
წარმოების თვალსაზრისით, ულტრაბგერის ერთ-ერთი ყველაზე მნიშვნელოვანი უპირატესობა მისი მასშტაბირებაა. ნანონაწილაკების წარმოების მრავალი ტექნიკისგან განსხვავებით, რომლებიც გეომეტრიის სპეციფიკურ პარტიულ პირობებზეა დამოკიდებული, ულტრაბგერითი დამუშავების მასშტაბირება შესაძლებელია მოცულობის ერთეულზე ენერგიის შეყვანის კონტროლით. ეს საშუალებას იძლევა, ლაბორატორიული მასშტაბით შემუშავებული პროცესები მაღალი შედარებადობით გადაიტანონ საპილოტე და სამრეწველო სისტემებში. ფარმაცევტული მწარმოებლებისთვის ეს მახასიათებელი ხელს უწყობს რეპროდუცირებადობას, ვალიდაციას და ტექნოლოგიების ეფექტურ გადაცემას განვითარების ეტაპებს შორის.
უწყვეტი ნაკადის სონიკაცია სამრეწველო წარმოებისთვის
ულტრაბგერითი ლიპოსომების დამუშავების ყველაზე სამრეწველო თვალსაზრისით შესაბამისი დანერგვა უწყვეტი ნაკადის ოპერაციაა. ნაკადის გზით ულტრაბგერითი უჯრედებში, ლიპოსომების დისპერსიები გადის განსაზღვრულ რეაქტორის მოცულობაში, ხოლო ულტრაბგერითი გამოიყენება კონტროლირებადი წნევის, ამპლიტუდის და ტემპერატურის ქვეშ. ეს კონფიგურაცია საშუალებას იძლევა ზუსტი კონტროლისთვის რეზიდენციის დროზე და ენერგიის ზემოქმედებაზე. პეპტიდებით დატვირთული ლიპოსომებისთვის, სადაც თერმული მგრძნობელობა და სტრუქტურული მთლიანობა კრიტიკულია, ასეთი კონტროლი აუცილებელია პროდუქტის ხარისხის შესანარჩუნებლად მასშტაბურად.
GLP-1-ისა და პეპტიდური თერაპიის ახალი თაობის შესაბამისობა
GLP-1 თერაპიების ორმაგი და მულტიაგონისტური პეპტიდებისკენ განვითარებასთან ერთად, მოსალოდნელია, რომ ფორმულირების სირთულე გაიზრდება. ამავდროულად, პაციენტების მოთხოვნა პერორალური ან ნაკლებად ინვაზიური მიწოდების გზებზე კვლავ იზრდება. შესაბამისად, მასშტაბირებადი მატარებლებზე დაფუძნებული მიწოდების პლატფორმები სტრატეგიულად მნიშვნელოვანი ხდება არა მხოლოდ ფარმაკოკინეტიკის გასაუმჯობესებლად, არამედ იმის უზრუნველსაყოფად, რომ ახალი პეპტიდური პრეპარატები საიმედოდ იქნას წარმოებული კომერციული მასშტაბით.
პეპტიდების პერორალური მიწოდების ფუნდამენტური ბარიერის მოგვარება
კუჭ-ნაწლავის ტრაქტი ბუნებით არაკეთილსაიმედოა პეპტიდების მიმართ და დაბალი ორალური ბიოშეღწევადობა ფუნდამენტურ ბარიერად რჩება მოწინავე ფორმულირებების შემთხვევაშიც კი. ლიპოსომული ინკაფსულაცია არ გამორიცხავს ამ გამოწვევას, მაგრამ ის უზრუნველყოფს რაციონალურ საინჟინრო მიდგომას დეგრადაციის შესამცირებლად და პეპტიდების ნაწლავის გარემოსთან ურთიერთქმედების კონტროლისთვის. მასშტაბირებად დამუშავების ტექნოლოგიებთან, როგორიცაა ულტრაბგერა, შერწყმისას, ლიპოსომებზე დაფუძნებული მიწოდების სისტემები უფრო ახლოს არის სამრეწველო განხორციელებადობასთან, ვიდრე ლაბორატორიულ ექსპერიმენტებთან შემოიფარგლება.
ლაბორატორიული განვითარებიდან სამრეწველო დანერგვამდე
 პრაქტიკული განვითარების სამუშაო პროცესებში, Hielscher Ultrasonics სისტემები ხშირად გამოიყენება, როგორც ულტრაბგერითი ლიპოსომის დამუშავების საცნობარო პლატფორმები. ლაბორატორიულ და ფორმულირების შემუშავების მასშტაბზე, კომპაქტური ულტრაბგერითი ზონდები, როგორიცაა UP200Ht და UP400St, საშუალებას იძლევა კონტროლირებადი მცირე პარტიების დამუშავებისა და მეთოდის ოპტიმიზაციისთვის. სამრეწველო წარმოებისთვის, ნაკადის რეაქტორებით აღჭურვილი სონიკატორები მხარს უჭერენ უწყვეტ მუშაობას, მაღალი სიმძლავრის სიმკვრივეს და წრფივ მასშტაბირებას. ეს მახასიათებლები შეესაბამება ფარმაცევტული წარმოების გარემოს მოთხოვნებს, მათ შორის პროცესის კონტროლს და რეპროდუცირებადობას.
პრაქტიკული განვითარების სამუშაო პროცესებში, Hielscher Ultrasonics სისტემები ხშირად გამოიყენება, როგორც ულტრაბგერითი ლიპოსომის დამუშავების საცნობარო პლატფორმები. ლაბორატორიულ და ფორმულირების შემუშავების მასშტაბზე, კომპაქტური ულტრაბგერითი ზონდები, როგორიცაა UP200Ht და UP400St, საშუალებას იძლევა კონტროლირებადი მცირე პარტიების დამუშავებისა და მეთოდის ოპტიმიზაციისთვის. სამრეწველო წარმოებისთვის, ნაკადის რეაქტორებით აღჭურვილი სონიკატორები მხარს უჭერენ უწყვეტ მუშაობას, მაღალი სიმძლავრის სიმკვრივეს და წრფივ მასშტაბირებას. ეს მახასიათებლები შეესაბამება ფარმაცევტული წარმოების გარემოს მოთხოვნებს, მათ შორის პროცესის კონტროლს და რეპროდუცირებადობას.
სემაგლუტიდის მიღმა: პლატფორმის პერსპექტივა
მიუხედავად იმისა, რომ სემაგლუტიდი წარმოადგენს უაღრესად რელევანტურ სამოდელო ნაერთს, ულტრაბგერითი ლიპოსომის კაფსულაციის შედეგები ვრცელდება ერთი API-ს მიღმა. იგივე პროცესის ლოგიკა ვრცელდება სხვა ლიპიდირებულ პეპტიდებზე, პეპტიდურ კონიუგატებსა და ახალ ბიოლოგიურ პრეპარატებზე. რადგან პეპტიდური თერაპიები ფართოვდება მეტაბოლურ დაავადებებში, ონკოლოგიასა და იმუნოლოგიაში, მასშტაბირებადი კაფსულაციის ტექნოლოგიები, სავარაუდოდ, გადამწყვეტი ფაქტორები გახდება იმის დასადგენად, თუ რომელი მიწოდების სტრატეგიები შეიძლება განვითარდეს კონცეფციიდან კომერციულ რეალობამდე.
პროცესით დამუშავებული პეპტიდების მიწოდებისკენ გადასვლა
ულტრაბგერით ინკაფსულირებული ლიპოსომური სემაგლუტიდი ფარმაცევტული განვითარების უფრო ფართო ცვლილებას ასახავს: ძირითადად ბიოლოგიური რაციონალობით განპირობებული ფორმულირების კონცეფციებიდან პროცესის ინჟინერიასა და წარმოებადობაზე დაფუძნებულ მიწოდების სისტემებამდე. სფეროში, სადაც მასშტაბირების დროს მრავალი ორალური პეპტიდური ტექნოლოგია ვერ ხერხდება, ულტრაბგერითი ლიპოსომური დამუშავება ლაბორატორიული განვითარებიდან სამრეწველო წარმოებამდე შედარებით პირდაპირ და ტექნიკურად მყარ გზას გვთავაზობს.
ლიტერატურა / ლიტერატურა
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
ხშირად დასმული შეკითხვები
რა არის GLP-1 პეპტიდები?
GLP-1 პეპტიდები ინკრეტინ-მიმეტიკური პეპტიდური პრეპარატებია, რომლებიც ააქტიურებენ გლუკაგონის მსგავს პეპტიდ-1 რეცეპტორს (GLP-1R), რომელიც წარმოადგენს ძირითად მეტაბოლურ რეცეპტორს, რომელიც მონაწილეობს გლუკოზა-დამოკიდებულ ინსულინის სეკრეციაში, გლუკაგონის გამოთავისუფლების დათრგუნვაში, კუჭის დაცლის შენელებასა და მადის რეგულაციაში. კლინიკურად გამოყენებული GLP-1 პეპტიდები (მაგალითად, სემაგლუტიდი) ქიმიურად მოდიფიცირებულია ფერმენტული დეგრადაციისადმი წინააღმდეგობის გასაწევად და ბუნებრივ GLP-1-თან შედარებით ცირკულაციის გახანგრძლივების მისაღწევად.
რა განსხვავებაა სემაგლუტიდსა და ტირზეპატიდს შორის?
სემაგლუტიდი არის ერთ-აგონისტი პეპტიდი, რომელიც შერჩევით ააქტიურებს გლუკაგონის მსგავს პეპტიდ-1 რეცეპტორს (GLP-1R), ხოლო ტირზეპატიდი არის ორმაგი აგონისტი, რომელიც ააქტიურებს როგორც GLP-1 რეცეპტორს, ასევე გლუკოზა-დამოკიდებულ ინსულინოტროპულ პოლიპეპტიდურ რეცეპტორს (GIPR). ბიოქიმიურად, ტირზეპატიდი არის უფრო დიდი და რთული პეპტიდი თანმიმდევრობის ელემენტებით და რეცეპტორ-შემაკავშირებელი დომენებით, რომლებიც ოპტიმიზირებულია ორი ინკრეტინის რეცეპტორის დასაკავშირებლად, ხოლო სემაგლუტიდი სპეციალურად შექმნილია მაღალი აფინურობის GLP-1R აქტივაციისთვის. ორივე პეპტიდი ქიმიურად მოდიფიცირებულია ლიპიდური ფრაგმენტებით, რათა გაიზარდოს პლაზმის ცილებთან შეკავშირება და გახანგრძლივდეს სისტემური ნახევარგამოყოფის პერიოდი, მაგრამ ტირზეპატიდის ორმაგი რეცეპტორული აქტივობა იწვევს უფრო ფართო მეტაბოლურ სიგნალიზაციას.
როგორ ხდება სემაგლუტიდის და ტირზეპატიდის ბიოქიმიური კლასიფიცირება?
სემაგლუტიდი ბიოქიმიურად კლასიფიცირდება, როგორც ხანგრძლივი მოქმედების, ლიპიდირებული GLP-1 რეცეპტორის აგონისტი პეპტიდი. ტირზეპატიდი კლასიფიცირდება, როგორც ხანგრძლივი მოქმედების, ლიპიდირებული ორმაგი ინკრეტინის რეცეპტორის აგონისტი პეპტიდი, კერძოდ, GLP-1R/GIPR კოაგონისტი.

Hielscher Ultrasonics აწარმოებს მაღალი ხარისხის ულტრაბგერითი ჰომოგენიზატორებისგან ლაბორატორია რომ სამრეწველო ზომა.