Liposomski semaglutid mogao bi biti sledeći veliki skok u isporuci lekova GLP-KSNUMKS
, Катхрин Хиелсцхер, objavljeno u Hielscher Nevs
GLP-1 peptidi kao što je semaglutid postali su jedan od najuticajnijih peptidnih terapeutika poslednje decenije, sa širokom kliničkom upotrebom kod dijabetesa tipa 2 i gojaznosti. Ipak, uprkos kliničkom uspehu, izazovi formulacije i proizvodnje semaglutida ostaju reprezentativni za peptidne lekove uopšte: oni su strukturno krhki, teško ih je zaštititi od degradacije i izuzetno je teško isporučiti neinvazivnim putevima. Ova ograničenja su glavni razlog zašto se većina agonista GLP-KSNUMKS receptora i dalje oslanja na injekcije, čak i kada potražnja za oralnom ili pacijentskom isporukom nastavlja da raste.
Granice trenutnih oralnih GLP-1 formulacija
Razvoj oralnih GLP-1 peptida pokazao je da je oralna isporuka tehnički moguća, ali je takođe izložio osnovna ograničenja postojećih strategija. Čak i u odobrenom proizvodu, oralni semaglutid pokazuje veoma nisku bioraspoloživost, obično ispod KSNUMKS%, što zahteva veće doziranje i doprinosi troškovima, varijabilnosti i složenosti formulacije. Ova ograničenja su pojačala interesovanje za sisteme zasnovane na nosačima koji mogu zaštititi peptidne lekove i potencijalno poboljšati apsorpciju bez oslanjanja isključivo na hemijske pojačivače permeacije.
Liposomi kao tehnički zrela platforma za isporuku
 Među sistemima isporuke koji se istražuju, liposomska enkapsulacija se izdvaja po svojoj tehničkoj zrelosti i farmaceutskom značaju. Liposomi se sastoje od fosfolipidnih dvoslojeva koji veoma liče na biološke membrane i imaju dugu istoriju kliničke upotrebe u onkologiji i infektivnim bolestima. Njihov značaj za peptidne terapije leži u njihovoj sposobnosti da fizički zaštite osetljive API-je, a istovremeno nude podesivu veličinu, sastav i površinska svojstva. Međutim, liposomske performanse snažno zavise od distribucije veličine, dvoslojne strukture, strategije učitavanja i ponovljivosti proizvodnje – faktori koji se prvenstveno regulišu procesnom tehnologijom, a ne samo sastavom formulacije.
Među sistemima isporuke koji se istražuju, liposomska enkapsulacija se izdvaja po svojoj tehničkoj zrelosti i farmaceutskom značaju. Liposomi se sastoje od fosfolipidnih dvoslojeva koji veoma liče na biološke membrane i imaju dugu istoriju kliničke upotrebe u onkologiji i infektivnim bolestima. Njihov značaj za peptidne terapije leži u njihovoj sposobnosti da fizički zaštite osetljive API-je, a istovremeno nude podesivu veličinu, sastav i površinska svojstva. Međutim, liposomske performanse snažno zavise od distribucije veličine, dvoslojne strukture, strategije učitavanja i ponovljivosti proizvodnje – faktori koji se prvenstveno regulišu procesnom tehnologijom, a ne samo sastavom formulacije.
Zašto je ultrazvučna obrada centralna za proizvodnju liposoma
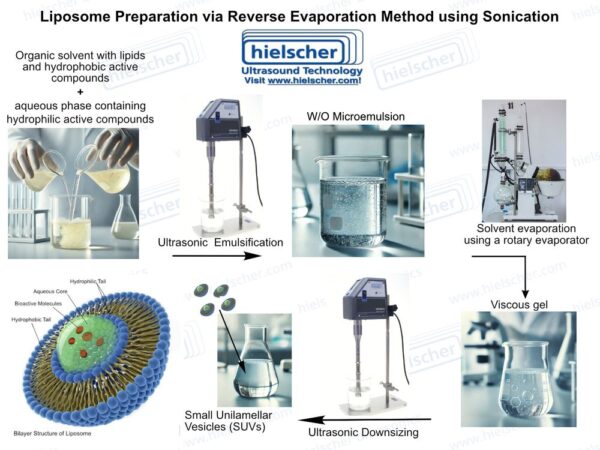
Ultrazvučna obrada se bavi nekoliko osnovnih izazova povezanih sa proizvodnjom liposoma. Ultrazvuk visokog intenziteta stvara akustičnu kavitaciju u tečnostima, stvarajući lokalizovane sile smicanja i efekte mikro-mešanja koji mogu razbiti lipidne agregate i pretvoriti multilamelarne strukture u manje, ujednačenije vezikule. U proizvodnji liposoma, ultrazvuk se može primeniti tokom formiranja vezikula ili kao korak naknadne obrade za standardizaciju veličine čestica i kvaliteta disperzije. Ova dvostruka uloga čini ultrazvuk posebno dragocenim u kontroli kritičnih atributa kvaliteta liposomskih sistema.
Strukturna kompatibilnost semaglutida sa lipidnim dvoslojima
GLP-1 peptidi kao što su semaglutid ili tirzepatid posebno su pogodni za nosače na bazi lipida, jer to nije jednostavan linearni peptid. Molekul sadrži hemijski modifikovani lipidni rep koji promoviše interakciju sa lipidnim membranama. Eksperimentalne studije koje su koristile sisteme vezikula pokazale su da se semaglutid i srodni peptidi mogu povezati sa membranama vezikula umetanjem ovog lipidnog repa. Iako su ovi nalazi dobijeni korišćenjem ekstracelularnih vezikula izvedenih iz mleka, a ne sintetičkih liposoma, osnovni mehanizam je direktno prenosiv. Lipidirani peptidi imaju inherentni afinitet za fosfolipidne dvoslojeve, što može poboljšati efikasnost punjenja i stabilnost formulacije bez potrebe za složenom hemijskom konjugacijom.
Uslovi procesa određuju efikasnost enkapsulacije
Kritički uvid iz nedavnih studija zasnovanih na vezikulama je da efikasnost enkapsulacije u velikoj meri zavisi od načina utovara i obrade. Ovo ima važne implikacije za farmaceutski razvoj: uspeh ili neuspeh formulacije peptidnih liposoma često manje zavisi od izbora lipida, a više od načina na koji se vezikule proizvode i obrađuju. Ultrazvučna obrada obezbeđuje kontrolisana i ponovljiva sredstva uticaja na ove parametre, što ga čini posebno atraktivnim za sistematski razvoj formulacije.
Skalabilnost kao ključna prednost ultrazvučne obrade
Sa stanovišta proizvodnje, jedna od najznačajnijih prednosti ultrazvuka je njegova skalabilnost. Za razliku od mnogih tehnika proizvodnje nanočestica koje se oslanjaju na uslove serije specifične za geometriju, ultrazvučna obrada se može skalirati kontrolom unosa energije po jedinici zapremine. Ovo omogućava da se procesi razvijeni u laboratorijskim razmerama prenesu na pilot i industrijske sisteme sa visokom uporedivošću. Za farmaceutske proizvođače, ova karakteristika podržava ponovljivost, validaciju i efikasan prenos tehnologije u razvojnim fazama.
Kontinuirano protok Sonication za industrijsku proizvodnju
Industrijski najrelevantnija implementacija ultrazvučne obrade liposoma je kontinuirani rad protoka. U ćelijama protoka kroz sonikaciju, liposomske disperzije prolaze kroz definisanu zapreminu reaktora, dok se ultrazvuk primenjuje pod kontrolisanim pritiskom, amplitudom i temperaturom. Ova konfiguracija omogućava preciznu kontrolu nad vremenom boravka i izloženosti energiji. Za liposome napunjene peptidima, gde su toplotna osetljivost i strukturni integritet kritični, takva kontrola je od suštinskog značaja za održavanje kvaliteta proizvoda na skali.
Relevantnost za sledeću generaciju GLP-1 i peptidne terapije
Kako se GLP-1 terapije razvijaju prema dual- i multi-agonističkim peptidima, očekuje se da će se složenost formulacije povećati. Istovremeno, potražnja pacijenata za oralnim ili manje invazivnim putevima isporuke nastavlja da raste. Skalabilne platforme za isporuku zasnovane na nosačima stoga postaju strateški važne, ne samo za poboljšanje farmakokinetike, već i za obezbeđivanje da se novi peptidni lekovi mogu pouzdano proizvoditi u komercijalnim razmerama.
Adresiranje osnovne barijere oralne isporuke peptida
Gastrointestinalni trakt je inherentno neprijateljski raspoložen prema peptidima, a niska oralna bioraspoloživost ostaje osnovna barijera čak i za napredne formulacije. Liposomska enkapsulacija ne eliminiše ovaj izazov, ali pruža racionalan inženjerski pristup za smanjenje degradacije i kontrolu načina na koji peptidi stupaju u interakciju sa crevnim okruženjima. U kombinaciji sa skalabilnim tehnologijama obrade kao što je ultrazvuk, sistemi isporuke na bazi liposoma približavaju se industrijskoj izvodljivosti, a ne ostaju ograničeni na laboratorijske eksperimente.
Od razvoja laboratorija do industrijske implementacije
 U praktičnim razvojnim tokovima rada, Hielscher Ultrasonics sistemi se često koriste kao referentne platforme za ultrazvučnu obradu liposoma. Na laboratorijskoj i razvojnoj skali, kompaktne ultrazvučne sonde kao što su UP200Ht i UP400St omogućavaju kontrolisanu obradu malih serija i optimizaciju metoda. Za industrijsku proizvodnju, zvučni uređaji opremljeni protočnim reaktorima podržavaju kontinuirani rad, visoku gustinu snage i linearno skaliranje. Ove karakteristike su u skladu sa zahtevima farmaceutskih proizvodnih okruženja, uključujući kontrolu procesa i ponovljivost.
U praktičnim razvojnim tokovima rada, Hielscher Ultrasonics sistemi se često koriste kao referentne platforme za ultrazvučnu obradu liposoma. Na laboratorijskoj i razvojnoj skali, kompaktne ultrazvučne sonde kao što su UP200Ht i UP400St omogućavaju kontrolisanu obradu malih serija i optimizaciju metoda. Za industrijsku proizvodnju, zvučni uređaji opremljeni protočnim reaktorima podržavaju kontinuirani rad, visoku gustinu snage i linearno skaliranje. Ove karakteristike su u skladu sa zahtevima farmaceutskih proizvodnih okruženja, uključujući kontrolu procesa i ponovljivost.
Iza semaglutida: perspektiva platforme
Iako semaglutid služi kao veoma relevantno jedinjenje modela, implikacije ultrazvučne inkapsulacije liposoma prevazilaze jedan API. Ista logika procesa važi i za druge lipidirane peptide, peptidne konjugate i nove biološke lekove. Kako se peptidne terapije šire preko metaboličkih bolesti, onkologije i imunologije, skalabilne tehnologije enkapsulacije će verovatno postati odlučujući faktori u određivanju koje strategije isporuke mogu napredovati od koncepta do komercijalne stvarnosti.
Pomak ka isporuci peptida projektovanog procesom
Liposomski semaglutid inkapsuliran ultrazvukom ilustruje širi pomak u farmaceutskom razvoju: od koncepata formulacije vođenih prvenstveno biološkim obrazloženjem prema sistemima isporuke zasnovanim na procesnom inženjeringu i proizvodnosti. U oblasti u kojoj mnoge oralne peptidne tehnologije ne uspevaju tokom skaliranja, ultrazvučna obrada liposoma nudi relativno direktan i tehnički robustan put od laboratorijskog razvoja do industrijske proizvodnje.
Литература / Референце
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
Често постављана питања
Šta su GLP-1 peptidi?
GLP-1 peptidi su inkretin-mimetički peptidni lekovi koji aktiviraju glukagonu sličan peptid-1 receptor (GLP-1R), ključni metabolički receptor koji je uključen u sekreciju insulina zavisnog od glukoze, suzbijanje oslobađanja glukagona, odloženo pražnjenje želuca i regulaciju apetita. Klinički korišćeni GLP-KSNUMKS peptidi (kao što je semaglutid) su hemijski modifikovani kako bi se oduprli enzimskoj razgradnji i postigli produženo vreme cirkulacije u poređenju sa izvornim GLP-KSNUMKS.
Koja je razlika između semaglutida i tirzepatida?
Semaglutid je peptid sa jednim agonistom koji selektivno aktivira receptor peptida-1 sličan glukagonu (GLP-1R), dok je tirzepatid dvostruki agonist koji aktivira i GLP-1 receptor i insulinotropni polipeptidni receptor (GIPR) zavisni od glukoze. Biohemijski, tirzepatid je veći i složeniji peptid sa elementima sekvence i domenima koji vezuju receptore optimizovani da angažuju dva inkretinska receptora, dok je semaglutid projektovan posebno za aktivaciju GLP-1R visokog afiniteta. Oba peptida su hemijski modifikovana lipidnim delovima kako bi se povećalo vezivanje proteina plazme i produžio sistemski poluživot, ali aktivnost dvostrukog receptora tirzepatida rezultira širom metaboličkom signalizacijom.
Kako su semaglutid i tirzepatid biohemijski klasifikovani?
Semaglutid je biohemijski klasifikovan kao lipidni peptid agonista GLP-KSNUMKS receptora dugog delovanja. Tirzepatid je klasifikovan kao lipidni peptid agonista dvostrukog inkretinskog receptora dugog delovanja, posebno kao koagonist GLP-1R / GIPR.

Хиелсцхер Ултрасоницс производи ултразвучне хомогенизаторе високих перформанси од лаб до индустријска величина.