סמגלוטייד ליפוזומלי עשוי להיות הקפיצה הגדולה הבאה בתחום מתן תרופות GLP-1
, קתרין היילשר, פורסם ב-Hielscher News
פפטידים מסוג GLP-1, כגון סמגלוטייד, הפכו לאחד הטיפולים הפפטידיים המשפיעים ביותר בעשור האחרון, עם שימוש קליני נרחב בסוכרת מסוג 2 והשמנת יתר. עם זאת, למרות הצלחתו הקלינית, האתגרים בגיבוש וייצור סמגלוטייד נותרו אופייניים לתרופות פפטידיות בכלל: הן שבירות מבחינה מבנית, קשות להגנה מפני פירוק, וקשות מאוד למתן בדרכים לא פולשניות. מגבלות אלה הן הסיבה העיקרית לכך שרוב אגוניסטים של קולטן GLP-1 עדיין מסתמכים על זריקות, גם כאשר הביקוש למתן דרך הפה או למתן ידידותי למטופל ממשיך לגדול.
מגבלות התכשירים הקיימים של GLP-1 לבליעה
פיתוח פפטידי GLP-1 אוראליים הוכיח כי מתן אוראלי הוא אפשרי מבחינה טכנית, אך הוא גם חשף את המגבלות המרכזיות של האסטרטגיות הקיימות. אפילו במוצר מאושר, סמגלוטייד אוראלי מציג זמינות ביולוגית נמוכה מאוד, בדרך כלל מתחת ל-1%, מה שמצריך מינון גבוה יותר ותורם לעלות, לשונות ולמורכבות התרכובת. מגבלות אלה הגבירו את העניין במערכות מבוססות נשא שיכולות להגן על תרופות פפטידיות ולשפר את הספיגה מבלי להסתמך באופן בלעדי על חומרים כימיים המשפרים את החדירות.
ליפוזומים כפלטפורמת העברה טכנולוגית בשלה
 מבין מערכות ההובלה הנחקרות, הכמוסה הליפוזומית בולטת בבגרותה הטכנולוגית וברלוונטיות התרופתית שלה. ליפוזומים מורכבים משכבות כפולות של פוספוליפידים הדומות מאוד לממברנות ביולוגיות, ויש להם היסטוריה ארוכה של שימוש קליני באונקולוגיה ובמחלות זיהומיות. הרלוונטיות שלהם לטיפול בפפטידים טמונה ביכולתם להגן פיזית על חומרים פעילים רגישים, תוך שהם מציעים גודל, הרכב ותכונות משטח הניתנים להתאמה. עם זאת, ביצועי הליפוזומים תלויים במידה רבה בפיזור הגודל, במבנה השכבה הכפולה, באסטרטגיית הטעינה ובשחזוריות הייצור. – גורמים הנשלטים בעיקר על ידי טכנולוגיית התהליך ולא רק על ידי הרכב התכשיר.
מבין מערכות ההובלה הנחקרות, הכמוסה הליפוזומית בולטת בבגרותה הטכנולוגית וברלוונטיות התרופתית שלה. ליפוזומים מורכבים משכבות כפולות של פוספוליפידים הדומות מאוד לממברנות ביולוגיות, ויש להם היסטוריה ארוכה של שימוש קליני באונקולוגיה ובמחלות זיהומיות. הרלוונטיות שלהם לטיפול בפפטידים טמונה ביכולתם להגן פיזית על חומרים פעילים רגישים, תוך שהם מציעים גודל, הרכב ותכונות משטח הניתנים להתאמה. עם זאת, ביצועי הליפוזומים תלויים במידה רבה בפיזור הגודל, במבנה השכבה הכפולה, באסטרטגיית הטעינה ובשחזוריות הייצור. – גורמים הנשלטים בעיקר על ידי טכנולוגיית התהליך ולא רק על ידי הרכב התכשיר.
מדוע עיבוד קולי הוא מרכזי בייצור ליפוזומים
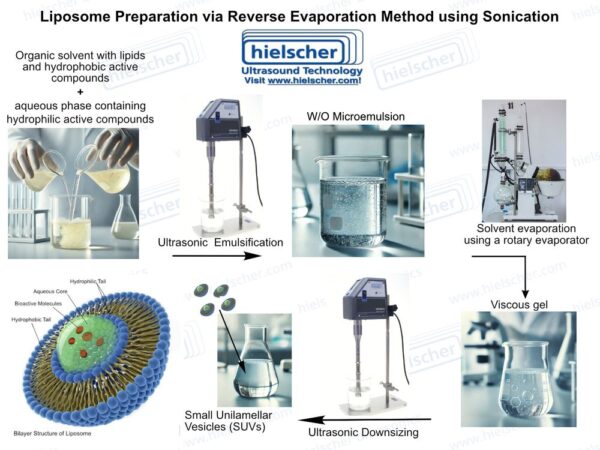
עיבוד קולי מטפל בכמה מהאתגרים המרכזיים הקשורים לייצור ליפוזומים. אולטרסאונד בעוצמה גבוהה יוצר קוויטציה אקוסטית בנוזלים, המייצרת כוחות גזירה מקומיים ואפקטים של ערבוב מיקרוסקופי, שיכולים לפרק מצבורי שומנים ולהמיר מבנים רב-שכביים לתאים קטנים ואחידים יותר. בייצור ליפוזומים, ניתן להשתמש באולטרסאונד במהלך היווצרות התאים או כשלב עיבוד לאחר הייצור, כדי לתקנן את גודל החלקיקים ואת איכות הפיזור. תפקיד כפול זה הופך את האולטרסאונד לכלי חשוב במיוחד בבקרת תכונות איכות קריטיות של מערכות ליפוזומליות.
תאימות מבנית של סמגלוטייד עם שכבות שומניות כפולות
פפטידים GLP-1 כגון semaglutide או tirzepatide מתאימים במיוחד למנשאים מבוססי שומנים, מכיוון שאינם פפטידים לינאריים פשוטים. המולקולה מכילה זנב שומני שעבר שינוי כימי, המסייע לאינטראקציה עם ממברנות שומניות. מחקרים ניסויים שבוצעו באמצעות מערכות של שלפוחיות הראו כי semaglutide ופפטידים קשורים יכולים להתחבר לממברנות השלפוחיות באמצעות החדרת זנב השומנים הזה. למרות שממצאים אלה הושגו באמצעות שלפוחיות תאיות שמקורן בחלב ולא באמצעות ליפוזומים סינתטיים, המנגנון הבסיסי ניתן להעברה ישירה. לפפטידים שומניים יש זיקה מובנית לשכבות כפולות של פוספוליפידים, מה שיכול לשפר את יעילות הטעינה ואת יציבות התרכובת ללא צורך בצימוד כימי מורכב.
תנאי התהליך קובעים את יעילות הכמוסה
תובנה קריטית ממחקרים אחרונים המבוססים על שלפוחיות היא שיעילות הכמוסה תלויה במידה רבה בשיטת הטעינה והעיבוד. יש לכך השלכות חשובות על פיתוח תרופות: הצלחתו או כישלונו של תרכובת ליפוזום פפטיד תלויה לעתים קרובות פחות בבחירת השומנים ויותר באופן ייצורן ועיבודן של השלפוחיות. עיבוד קולי מספק אמצעי ניתן לשליטה וניתן לשחזור להשפעה על פרמטרים אלה, מה שהופך אותו לאטרקטיבי במיוחד לפיתוח שיטתי של תרכובות.
מדרגיות כיתרון מרכזי של עיבוד קולי
מנקודת מבט ייצורית, אחד היתרונות המשמעותיים ביותר של אולטרסאונד הוא יכולת ההרחבה שלו. בניגוד לטכניקות ייצור ננו-חלקיקים רבות, התלויות בתנאי ייצור ספציפיים לגיאומטריה, ניתן להגדיל את היקף העיבוד האולטרסוני על ידי בקרת צריכת האנרגיה ליחידת נפח. הדבר מאפשר להעביר תהליכים שפותחו בקנה מידה מעבדתי למערכות פיילוט ותעשייתיות עם רמת השוואתיות גבוהה. עבור יצרני תרופות, מאפיין זה תומך בשחזור, אימות והעברת טכנולוגיה יעילה בין שלבי הפיתוח.
סוניקציה בזרימה רציפה לייצור תעשייתי
היישום התעשייתי הרלוונטי ביותר של עיבוד ליפוזומים באמצעות אולטרסאונד הוא פעולה בזרימה רציפה. בתאי סוניקציה בזרימה רציפה, פיזור הליפוזומים עובר בנפח מוגדר של הכור, תוך הפעלת אולטרסאונד בלחץ, משרעת וטמפרטורה מבוקרים. תצורה זו מאפשרת שליטה מדויקת על זמן השהייה וחשיפה לאנרגיה. עבור ליפוזומים עתירי פפטידים, שבהם הרגישות התרמית והשלמות המבנית הן קריטיות, שליטה כזו היא חיונית לשמירה על איכות המוצר בקנה מידה גדול.
רלוונטיות לדור הבא של GLP-1 וטיפול פפטידי
עם התפתחות טיפולי GLP-1 לכיוון פפטידים דו-אגוניסטים ורב-אגוניסטים, צפוי כי מורכבות התרכובות תגדל. במקביל, הביקוש של המטופלים לטיפול דרך הפה או בדרכים פחות פולשניות ממשיך לגדול. לפיכך, פלטפורמות מתקדמות מבוססות נשא הופכות להיות בעלות חשיבות אסטרטגית, לא רק לשיפור הפרמקוקינטיקה, אלא גם להבטחת ייצור אמין של תרופות פפטידיות חדשות בקנה מידה מסחרי.
התמודדות עם המחסום הבסיסי של העברת פפטידים דרך הפה
מערכת העיכול היא מטבעה עוינת לפפטידים, וזמינות ביולוגית נמוכה דרך הפה נותרת מכשול מהותי אפילו עבור תכשירים מתקדמים. אנקפסולציה ליפוזומית אינה מבטלת את האתגר הזה, אך היא מספקת גישה הנדסית רציונלית להפחתת הפירוק ולבקרה על האופן שבו הפפטידים מקיימים אינטראקציה עם סביבות המעי. בשילוב עם טכנולוגיות עיבוד הניתנות להרחבה, כגון אולטרסאונד, מערכות העברה מבוססות ליפוזומים מתקרבות לישימות תעשייתית במקום להישאר מוגבלות לניסויים במעבדה.
מפיתוח במעבדה ליישום תעשייתי
 בתהליכי פיתוח מעשיים, מערכות Hielscher Ultrasonics משמשות לעתים קרובות כפלטפורמות ייחוס לעיבוד ליפוזומים באמצעות אולטרסאונד. במעבדות ובפיתוח פורמולות, בדיקות קומפקטיות באמצעות אולטרסאונד כגון UP200Ht ו-UP400St מאפשרות עיבוד מבוקר של כמויות קטנות ואופטימיזציה של השיטה. בייצור תעשייתי, מכשירי סוניקציה המצוידים במתקני זרימה תומכים בפעולה רציפה, בצפיפות הספק גבוהה ובהגדלה ליניארית. מאפיינים אלה תואמים את הדרישות של סביבות ייצור תרופות, כולל בקרת תהליכים ושחזור.
בתהליכי פיתוח מעשיים, מערכות Hielscher Ultrasonics משמשות לעתים קרובות כפלטפורמות ייחוס לעיבוד ליפוזומים באמצעות אולטרסאונד. במעבדות ובפיתוח פורמולות, בדיקות קומפקטיות באמצעות אולטרסאונד כגון UP200Ht ו-UP400St מאפשרות עיבוד מבוקר של כמויות קטנות ואופטימיזציה של השיטה. בייצור תעשייתי, מכשירי סוניקציה המצוידים במתקני זרימה תומכים בפעולה רציפה, בצפיפות הספק גבוהה ובהגדלה ליניארית. מאפיינים אלה תואמים את הדרישות של סביבות ייצור תרופות, כולל בקרת תהליכים ושחזור.
מעבר לסמגלוטייד: פרספקטיבה פלטפורמית
בעוד שסמגלוטייד משמש כתרכובת מודל רלוונטית ביותר, ההשלכות של קפסולת ליפוזום אולטראסונית חורגות מעבר ל-API בודד. אותו היגיון תהליכי חל גם על פפטידים ליפידים אחרים, קונג'וגטים פפטידיים ותרופות ביולוגיות חדשות. ככל שתרופות פפטידיות מתפשטות לתחומים של מחלות מטבוליות, אונקולוגיה ואימונולוגיה, טכנולוגיות קפסולת מדרגיות צפויות להפוך לגורמים מכריעים בקביעת אילו אסטרטגיות מתן תרופות יוכלו להתקדם משלב הרעיון לשלב המסחרי.
מעבר להעברת פפטידים באמצעות הנדסת תהליכים
סמגלוטייד ליפוזומלי מוקפסול באולטרסאונד מדגים שינוי רחב יותר בפיתוח התרופות: מתפיסות פורמולציה המונעות בעיקר על ידי היגיון ביולוגי למערכות אספקה המבוססות על הנדסת תהליכים ויכולת ייצור. בתחום שבו טכנולוגיות פפטיד אוראליות רבות נכשלות במהלך ההרחבה, עיבוד ליפוזומים באולטרסאונד מציע מסלול ישיר יחסית וטכני חזק מהפיתוח במעבדה ועד הייצור התעשייתי.
ספרות / מקורות
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
שאלות נפוצות
מהם פפטידים GLP-1?
פפטידי GLP-1 הם תרופות פפטידיות המדמות אינקרטינים, המפעילות את הקולטן לפפטיד דמוי גלוקגון-1 (GLP-1R), קולטן מטבולי מרכזי המעורב בהפרשת אינסולין תלוית גלוקוז, דיכוי שחרור גלוקגון, עיכוב ריקון הקיבה וויסות התיאבון. פפטידי GLP-1 המשמשים קלינית (כגון semaglutide) עוברים שינוי כימי כדי לעמוד בפני פירוק אנזימטי ולהשיג זמן מחזור ממושך יותר בהשוואה ל-GLP-1 טבעי.
מה ההבדל בין סמגלוטייד לטיירזפטייד?
Semaglutide הוא פפטיד אגוניסט יחיד המפעיל באופן סלקטיבי את הקולטן לפפטיד דמוי גלוקגון-1 (GLP-1R), בעוד ש-tirzepatide הוא אגוניסט כפול המפעיל הן את הקולטן GLP-1 והן את הקולטן לפוליפפטיד אינסולינוטרופי תלוי גלוקוז (GIPR). מבחינה ביוכימית, טירזפטיד הוא פפטיד גדול ומורכב יותר, עם אלמנטים רצפיים ותחומים קשירת קולטנים המותאמים באופן מיטבי לקשירת שני קולטני אינקרטינים, בעוד סמגלוטייד תוכנן במיוחד להפעלת GLP-1R בעלת זיקה גבוהה. שני הפפטידים עברו שינוי כימי עם קבוצות שומניות כדי להגביר את קשירת החלבון בפלסמה ולהאריך את מחצית החיים המערכתית, אך פעילות הקולטן הכפול של טירזפטיד מובילה לאיתות מטבולי רחב יותר.
כיצד מסווגים סמגלוטייד וטירזפטייד מבחינה ביוכימית?
Semaglutide מסווג ביוכימית כפפטיד אגוניסט של קולטן GLP-1 ארוך טווח, משומן. Tirzepatide מסווג כפפטיד אגוניסט של קולטן אינקרטיני כפול ארוך טווח, משומן, ובאופן ספציפי כקואגוניסט של GLP-1R/GIPR.

Hielscher Ultrasonics מייצרת הומוגנייזרים קוליים בעלי ביצועים גבוהים מ המעבדה ל גודל תעשייתי.