Липосомальный семаглутид может стать следующим большим скачком в доставке препаратов GLP-1
, Катрин ХильшерОпубликовано в журнале Hielscher News
Пептиды GLP-1, такие как семаглутид, стали одним из самых влиятельных пептидных препаратов последнего десятилетия, получив широкое клиническое применение при диабете 2 типа и ожирении. Однако, несмотря на клинический успех семаглутида, проблемы с его разработкой и производством остаются характерными для пептидных препаратов в целом: они структурно хрупки, их трудно защитить от деградации, и, как известно, их трудно доставлять неинвазивными способами. Эти ограничения являются основной причиной того, что большинство агонистов рецепторов GLP-1 по-прежнему применяются в виде инъекций, даже несмотря на растущий спрос на пероральные или удобные для пациентов способы доставки.
Предельные возможности существующих пероральных препаратов GLP-1
Разработка пероральных пептидов GLP-1 показала, что пероральная доставка технически возможна, но также выявила основные ограничения существующих стратегий. Даже в одобренном препарате пероральный семаглутид демонстрирует очень низкую биодоступность, обычно менее 1 %, что требует более высокой дозировки и приводит к удорожанию, изменчивости и сложности рецептуры. Эти ограничения усилили интерес к системам на основе носителей, которые могут защитить пептидные препараты и потенциально улучшить всасывание, не полагаясь исключительно на химические усилители проницаемости.
Липосомы как технически зрелая платформа доставки
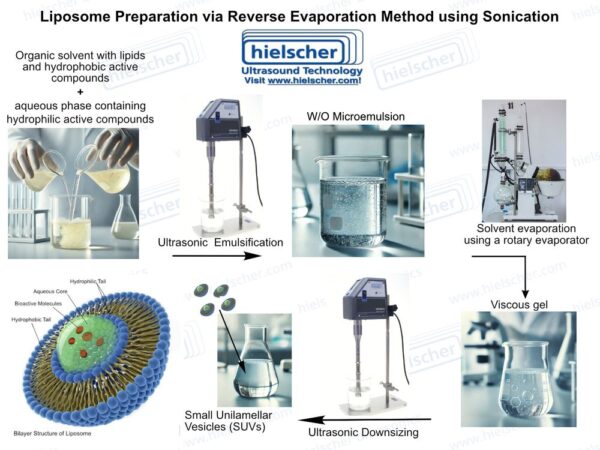
 Среди исследуемых систем доставки липосомальная инкапсуляция выделяется своей технической зрелостью и фармацевтической актуальностью. Липосомы состоят из фосфолипидных бислоев, которые очень похожи на биологические мембраны, и имеют долгую историю клинического применения в онкологии и инфекционных заболеваниях. Их актуальность для пептидной терапии заключается в способности физически защищать чувствительные API, обеспечивая при этом регулируемый размер, состав и свойства поверхности. Однако эффективность липосом сильно зависит от распределения размеров, структуры бислоя, стратегии загрузки и воспроизводимости производства. – факторы, которые в первую очередь зависят от технологии процесса, а не только от состава рецептуры.
Среди исследуемых систем доставки липосомальная инкапсуляция выделяется своей технической зрелостью и фармацевтической актуальностью. Липосомы состоят из фосфолипидных бислоев, которые очень похожи на биологические мембраны, и имеют долгую историю клинического применения в онкологии и инфекционных заболеваниях. Их актуальность для пептидной терапии заключается в способности физически защищать чувствительные API, обеспечивая при этом регулируемый размер, состав и свойства поверхности. Однако эффективность липосом сильно зависит от распределения размеров, структуры бислоя, стратегии загрузки и воспроизводимости производства. – факторы, которые в первую очередь зависят от технологии процесса, а не только от состава рецептуры.
Почему ультразвуковая обработка занимает центральное место в производстве липосом
Ультразвуковая обработка позволяет решить несколько основных проблем, связанных с производством липосом. Ультразвук высокой интенсивности вызывает акустическую кавитацию в жидкости, создавая локальные сдвиговые силы и эффекты микроперемешивания, которые могут разрушать липидные агрегаты и превращать мультиламеллярные структуры в более мелкие и однородные везикулы. При производстве липосом ультразвук может применяться как во время формирования везикул, так и на этапе последующей обработки для стандартизации размера частиц и качества дисперсии. Эта двойная роль делает ультразвук особенно ценным для контроля критических атрибутов качества липосомальных систем.
Структурная совместимость семаглутида с липидными билайерами
Пептиды GLP-1, такие как семаглутид или тирзепатид, особенно хорошо подходят для носителей на основе липидов, поскольку это не простой линейный пептид. Молекула содержит химически модифицированный липидный хвост, который способствует взаимодействию с липидными мембранами. Экспериментальные исследования с использованием систем везикул показали, что семаглутид и родственные ему пептиды могут связываться с мембранами везикул благодаря вставке этого липидного хвоста. Хотя эти результаты были получены на основе внеклеточных везикул, полученных из молока, а не синтетических липосом, механизм, лежащий в их основе, можно напрямую перенести на другие системы. Липидированные пептиды обладают врожденным сродством к фосфолипидным бислоям, что может повысить эффективность загрузки и стабильность состава без необходимости сложной химической конъюгации.
Условия процесса определяют эффективность инкапсуляции
Важнейший вывод, сделанный в ходе недавних исследований везикул, заключается в том, что эффективность инкапсуляции в значительной степени зависит от способа загрузки и обработки. Это имеет важные последствия для фармацевтической разработки: успех или неудача пептидной липосомной формулы часто зависит не столько от выбора липида, сколько от способа производства и обработки везикул. Ультразвуковая обработка обеспечивает контролируемый и воспроизводимый способ влияния на эти параметры, что делает ее особенно привлекательной для систематической разработки рецептур.
Масштабируемость как ключевое преимущество ультразвуковой обработки
С точки зрения производства, одним из наиболее значимых преимуществ ультразвука является его масштабируемость. В отличие от многих технологий производства наночастиц, которые зависят от геометрических условий партии, ультразвуковую обработку можно масштабировать, контролируя потребление энергии на единицу объема. Это позволяет переносить процессы, разработанные в лабораторных масштабах, на пилотные и промышленные системы с высокой степенью сопоставимости. Для фармацевтических производителей эта характеристика способствует воспроизводимости, валидации и эффективному переносу технологий на разных этапах разработки.
Непрерывное поточное сонирование для промышленного производства
Наиболее актуальной для промышленности реализацией ультразвуковой обработки липосом является непрерывный поток. В проточных соникационных камерах липосомные дисперсии проходят через определенный объем реактора, в то время как ультразвук подается под контролируемым давлением, амплитудой и температурой. Такая конфигурация позволяет точно контролировать время пребывания и энергетическое воздействие. Для липосом, нагруженных пептидами, где термочувствительность и структурная целостность имеют решающее значение, такой контроль необходим для поддержания качества продукта в масштабах производства.
Актуальность для GLP-1 и пептидных препаратов нового поколения
По мере развития терапии GLP-1 в сторону пептидов с двумя и несколькими агонистами ожидается увеличение сложности рецептур. В то же время спрос пациентов на пероральные или менее инвазивные способы доставки продолжает расти. Поэтому масштабируемые платформы доставки на основе носителей становятся стратегически важными не только для улучшения фармакокинетики, но и для обеспечения надежного производства новых пептидных препаратов в коммерческих масштабах.
Преодоление фундаментального барьера пероральной доставки пептидов
Желудочно-кишечный тракт по своей природе враждебен для пептидов, и низкая пероральная биодоступность остается основным барьером даже для современных препаратов. Липосомальное инкапсулирование не устраняет эту проблему, но обеспечивает рациональный инженерный подход к снижению деградации и контролю взаимодействия пептидов с кишечной средой. В сочетании с масштабируемыми технологиями обработки, такими как ультразвук, системы доставки на основе липосом приближаются к промышленной осуществимости, а не остаются в рамках лабораторных экспериментов.
От лабораторных разработок до промышленного внедрения
 В практических разработках системы Hielscher Ultrasonics часто используются в качестве эталонных платформ для ультразвуковой обработки липосом. В лабораторных условиях и при разработке рецептур компактные ультразвуковые датчики, такие как UP200Ht и UP400St, позволяют проводить контролируемую мелкосерийную обработку и оптимизировать методы. Для промышленного производства ультразвуковые датчики, оснащенные проточными реакторами, поддерживают непрерывную работу, высокую плотность мощности и линейное масштабирование. Эти характеристики соответствуют требованиям фармацевтического производства, включая контроль и воспроизводимость процесса.
В практических разработках системы Hielscher Ultrasonics часто используются в качестве эталонных платформ для ультразвуковой обработки липосом. В лабораторных условиях и при разработке рецептур компактные ультразвуковые датчики, такие как UP200Ht и UP400St, позволяют проводить контролируемую мелкосерийную обработку и оптимизировать методы. Для промышленного производства ультразвуковые датчики, оснащенные проточными реакторами, поддерживают непрерывную работу, высокую плотность мощности и линейное масштабирование. Эти характеристики соответствуют требованиям фармацевтического производства, включая контроль и воспроизводимость процесса.
За пределами семаглутида: Перспектива платформы
Хотя семаглутид служит весьма актуальным модельным соединением, последствия ультразвукового липосомного инкапсулирования выходят за рамки одного API. Та же логика процесса применима к другим липидированным пептидам, пептидным конъюгатам и новым биопрепаратам. По мере развития пептидной терапии в области метаболических заболеваний, онкологии и иммунологии масштабируемые технологии инкапсуляции, вероятно, станут решающими факторами в определении того, какие стратегии доставки смогут перейти от концепции к коммерческой реальности.
Сдвиг в сторону процессно-инженерной доставки пептидов
Капсулированный ультразвуком липосомальный семаглутид иллюстрирует более широкий сдвиг в фармацевтической разработке: от концепций рецептур, основанных в первую очередь на биологическом обосновании, к системам доставки, основанным на технологическом проектировании и технологичности. В области, где многие пероральные пептидные технологии терпят неудачу при масштабировании, ультразвуковая обработка липосом предлагает сравнительно прямой и технически надежный путь от лабораторной разработки до промышленного производства.
Литература / Литература
- M.E. Barbinta-Patrascu, N. Badea, M. Constantin, C. Ungureanu, C. Nichita, S.M. Iordache, A. Vlad, S. Antohe (2018): Bio-Activity of Organic/Inorganic Photo-Generated Composites in Bio-Inspired Systems. Romanian Journal of Physics 63, 702 (2018).
- Raquel Martínez-González, Joan Estelrich, Maria Antònia Busquets (2016): Liposomes Loaded with Hydrophobic Iron Oxide Nanoparticles: Suitable T2 Contrast Agents for MRI. International Journal of Molecular Science 2016.
- Shah Purvin, Parameswara Rao Vuddanda, Sanjay Kumar Singh, Achint Jain, and Sanjay Singh (2014): Pharmacokinetic and Tissue Distribution Study of Solid Lipid Nanoparticles of Zidov in Rats. Journal of Nanotechnology, Volume 2014.
- Harshita Krishnatreyya, Sanjay Dey, Paulami Pal, Pranab Jyoti Das, Vipin Kumar Sharma, Bhaskar Mazumder (2019): Piroxicam Loaded Solid Lipid Nanoparticles (SLNs): Potential for Topical Delivery. Indian Journal of Pharmaceutical Education and Research Vol 53, Issue 2, 2019. 82-92.
Часто задаваемые вопросы
Что такое пептиды GLP-1?
Пептиды GLP-1 - это инкретин-миметические пептидные препараты, которые активируют рецептор глюкагоноподобного пептида-1 (GLP-1R), ключевой метаболический рецептор, участвующий в глюкозозависимой секреции инсулина, подавлении выброса глюкагона, задержке опорожнения желудка и регуляции аппетита. Клинически используемые пептиды GLP-1 (например, семаглутид) химически модифицированы, чтобы противостоять ферментативной деградации и достичь более длительного времени циркуляции по сравнению с нативным GLP-1.
В чем разница между семаглутидом и тирзепатидом?
Семаглутид - одноагонистический пептид, избирательно активирующий рецептор глюкагоноподобного пептида-1 (GLP-1R), в то время как тирзепатид - двойной агонист, активирующий как рецептор GLP-1, так и рецептор глюкозозависимого инсулинотропного полипептида (GIPR). Биохимически тирзепатид представляет собой более крупный и сложный пептид с элементами последовательности и рецептор-связывающими доменами, оптимизированными для задействования двух инкретиновых рецепторов, в то время как семаглутид разработан специально для высокоаффинной активации GLP-1R. Оба пептида химически модифицированы липидными соединениями для повышения связывания с белками плазмы и увеличения системного периода полураспада, но двухрецепторная активность тирзепатида приводит к более широкому метаболическому сигналу.
Как биохимически классифицируются семаглутид и тирзепатид?
По биохимическим показателям семаглутид относится к пептидам длительного действия, липидированным агонистам рецепторов GLP-1. Тирзепатид классифицируется как пептид длительного действия, липидированный двойной агонист инкретиновых рецепторов, в частности, коагонист GLP-1R/GIPR.

Hielscher Ultrasonics производит высокопроизводительные ультразвуковые гомогенизаторы от лаборатория Кому промышленного размера.